Quando abordamos um doente com o diagnóstico de taquiarritmia ventricular, devemos, de forma sistemática, procurar a presença de alterações cardíacas estruturais (sendo a mais frequente etiologia a doença coronária), uma vez que esse facto tem implicações prognósticas e terapêuticas importantes.
Existe um subgrupo de doentes, nos quais, a taquicardia ventricular, surge em coração estruturalmente normal, sendo habitualmente designada de taquicardia ventricular idiopática. Estima‐se que este subgrupo possa corresponder até 10% dos casos de taquicardia ventricular1.
Nestes doentes, são frequentemente utilizados dois tipos de tratamento, o farmacológico e a ablação por cateter (ou ambos em simultâneo). No entanto, destaca‐se que, uma vez que estas arritmias são focais, são acessíveis a tratamento com elevadas taxas de sucesso, através de ablação por cateter2.
Desde a primeira descrição sistemática no início da década de 80 do século XX, de taquicardias com origem na câmara de saída do ventrículo direito, por Buxton3, o conhecimento sobre as taquicardias ventriculares idiopáticas tem aumentado francamente.
Por exemplo, no que respeita aos mecanismos fisiopatológicos, Lerman, et al. publicaram diversos trabalhos4‐6, nos quais demonstraram que a maioria das taquicardias com origem na região da câmara de saída do ventrículo direito, são sensíveis à adenosina e que os mecanismos eletrofisiológicos mais prováveis serão a ocorrência de pós‐potenciais tardios e as pós‐despolarizações tardias mediados por estimulação catecolaminérgica e a atividade deflagrada (triggered), sendo estas alterações eletrofisiológicas associadas a sobrecarga de cálcio intracelular7.
Dado o contexto fisiopatológico intracelular, compreende‐se que, no laboratório de eletrofisiologia, este tipo de taquicardia seja induzida com a utilização de isoprenalina, aminofilina, atropina e estimulação com pacing rápido mas não (ou raramente) com a estimulação ventricular programada8.
As taquicardias da câmara de saída ventricular compreendem um subgrupo destas taquicardias idiopáticas, que predominantemente se localizam no tecido miocárdico dos tratos de saída do ventrículo direito e do ventrículo esquerdo.
Em 80 a 90% dos casos, a taquicardia origina‐se na câmara de saída do ventrículo direito9.
Globalmente, o prognóstico é favorável, embora o médico deva permanecer atento, uma vez que em alguns casos se verifica uma evolução para disfunção do ventrículo esquerdo (taquicardiomiopatia induzida)10, estando também descritos casos raros de variantes malignas11.
Uma componente essencial no diagnóstico é a cuidadosa análise eletrocardiográfica, uma vez que este exame permite‐nos identificar com particular acuidade o local de origem da arritmia, definindo se tem origem no ventrículo direito ou no esquerdo (essencialmente de acordo com a morfologia do complexo QRS nas derivações pré‐cordiais direitas) e até em que região segmentar do trato de saída12.
A grande evolução tecnológica ao dispor da Cardiologia, veio tornar cada vez mais importante o conhecimento primordial da anatomia.
Observando‐se o tórax em posição frontal, o ventrículo direito constitui a câmara cardíaca de posição mais anterior, localizando‐se imediatamente sob o esterno. A aurícula direita é anterior enquanto a aurícula esquerda é a câmara mais posterior do coração.
Comparativamente com a morfologia cónica do ventrículo esquerdo, o ventrículo direito possui uma forma mais triangular13.
Tanto o ventrículo direito como o esquerdo, são descritos como dividindo‐se em três componentes: a região/câmara de entrada, a região apical trabecular e a câmara de saída (trato de saída)14.
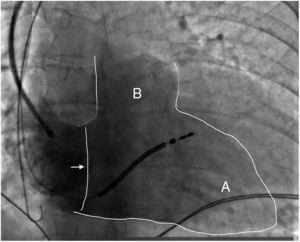
Na figura 1 conseguimos identificar estas três regiões descritas, podendo facilmente observar‐se a existência de uma região que se apresenta quase «separada» do restante ventrículo direito (assinalada com a letra B), correspondendo à região da câmara de saída do ventrículo direito (ou infundibulum).
Imagem radioscópica, em incidência Oblíqua Anterior Direita (OAD) a 30°, com a visualização de contraste no ventrículo direito, permitindo a identificação (delineada a branco) da região da Válvula Tricúspide (seta), Região Apical do Ventrículo Direito (A) e Câmara de Saída do Ventrículo direito (B). Pode observar‐se também a presença de eletrocateter de Cardioversor‐Desfibrilhador de fixação ativa, cuja ponta se encontra na região septal supero‐mediana (Silva Cunha P., Oliveira M.).
Neste número da Revista Portuguesa de Cardiologia é publicado um estudo de Parreira, et al.16 que – apesar de incluir um número reduzido de doentes – se nos afigura interessante e útil do ponto de vista clínico.
Estes autores decidiram examinar, num grupo de 18 doentes com extrassistolia (> 10 000 sístoles ventriculares prematuras nas 24h) – com origem provável na câmara de saída do ventrículo direito –, a correlação entre os achados eletrocardiográficos e os achados da avaliação intracavitária invasiva durante o estudo eletrofisiológico, com a medição da voltagem tecidular local.
Antes do início do estudo eletrofisiológico, os autores efetuaram um segundo eletrocardiograma, no qual as derivações do plano frontal V1 e V2 foram colhidas no 2.° espaço intercostal, com o objetivo de recolher de forma mais precisa a atividade elétrica da câmara de saída do ventrículo direito (dada a localização desta região anatómica, como explicado anteriormente).
Neste 2.° eletrocardiograma observaram a presença de elevação do segmento ST em um terço dos doentes, correlacionando‐se esta alteração eletrocardiográfica com a presença de áreas de baixa voltagem na câmara de saída do ventrículo direito.
Sabemos que, como verificado em diversos estudos já publicados, o eletrocardiograma obtido numa posição mais alta do que a convencional (no 2.° ou 3.° espaço intercostal) é vantajoso na deteção de alterações do ventrículo direito, podendo, por exemplo, aumentar a sensibilidade diagnóstica em casos de suspeita de Síndrome de Brugada15.
Do ponto de vista de exclusão rigorosa de presença de cardiopatia estrutural, o estudo de Parreira, et al., apresenta algumas limitações, uma vez que nem todos os doentes foram estudados com ressonância magnética cardíaca, de forma a excluir a presença de fibrose miocárdica regional.
Ainda assim, consideramos importante neste estudo a identificação através do eletrocardiograma de alterações patológicas regionais, que têm objetivação no mapeamento tridimensional intracavitário (áreas de baixa voltagem) em doentes com coração aparentemente sem alterações estruturais.
Estes dados fazem‐nos supor que em diversos casos classificados na literatura mundial, como de taquicardias idiopáticas do ventrículo direito – e por isso sem alterações estruturais associadas – essas mesmas alterações estruturais, na verdade, existem (ainda em fase incipiente), mas ainda não foram alcançadas ferramentas diagnósticas suficientemente sensíveis para a sua identificação.
Neste estudo, as alterações do segmento ST e a presença de áreas de baixa voltagem, não se correlacionaram, ainda assim, com o sucesso agudo da ablação ou com a taxa de recorrência.
Seria também relevante, que os autores tivessem tentado responder à interrogação de se existirá um valor mínimo de área anatómica de baixa voltagem, que se correlacione com as alterações ECG, apresentando os dados da medição das áreas totais de baixa voltagem.
Não obstante algumas das limitações metodológicas referidas, às quais acresce o facto de a avaliação ser efetuada com dois diferentes sistemas de mapeamento tridimensional, exortamos os autores a prosseguirem esta linha de investigação.
Conflito de interessesO autor declara não haver conflito de interesses.