A dislipidemia aterogénica contribui consideravelmente para o risco residual de doença cardiovascular (DCV); não obstante, esta patologia encontra‐se subdiagnosticada e submedicada. O objetivo deste estudo foi analisar a opinião dos especialistas portugueses e gerar um consenso sobre o diagnóstico e o tratamento da dislipidemia aterogénica, bem como promover a uniformização da prática clínica neste contexto.
MétodosEste estudo consistiu na aplicação de um questionário a um painel de peritos seguindo uma metodologia Delphi modificada.
ResultadosA maioria dos itens (88,4%) foi consensual. Os peritos inquiridos mostraram reconhecer a importância da dislipidemia aterogénica, o papel preponderante do colesterol de lipoproteínas de baixa densidade (c‐LDL) e do colesterol total, excluindo o das lipoproteínas de alta densidade (colesterol não‐HDL), na indicação do risco cardiovascular e na definição de objetivos terapêuticos, a eleição das estatinas como fármaco antidislipidémico de primeira linha e a pertinência da sua associação com o fenofibrato para a redução do risco residual. Não obstante, o painel manifestou incerteza no que se refere ao papel dos triglicerídeos e ao valor terapêutico dos fibratos. Tendo como base a evidência disponível na literatura e as opiniões recolhidas neste estudo, a comissão científica elaborou um algoritmo de tratamento com o objetivo de promover a sensibilização e adequação da terapêutica a doentes com dislipidemia aterogénica.
ConclusõesOs inquiridos mostraram estar familiarizados com o conceito e com a importância da dislipidemia aterogénica; as poucas situações de ausência de consenso poderão estar relacionadas com uma diferente interpretação e/ou valorização da evidência científica disponível.
Atherogenic dyslipidemia is an important contributor to residual cardiovascular (CV) risk, but it is underdiagnosed and undertreated. This study aimed to assess the opinion of Portuguese experts to generate a consensus concerning the diagnosis and treatment of atherogenic dyslipidemia, as well as to contribute toward standardization of clinical practice in this disorder.
MethodsThe study consisted in the application of a questionnaire to an expert panel, following a modified Delphi methodology.
ResultsThe majority (88.4%) of the proposed items were found to be consensual. The expert panel recognized the importance of the atherogenic dyslipidemia phenotype, the role played by low‐density lipoprotein cholesterol and non‐high‐density lipoprotein cholesterol as risk markers and therapeutic targets, the choice of statins as first‐line lipid‐lowering drugs, and the value of associating statins with fenofibrate as a means to reduce residual CV risk. However, the role played by triglycerides in CV risk and the therapeutic value of fibrates lacked consensus. Taking into consideration the state of the art and the opinions expressed in this study, the scientific committee developed a treatment algorithm aimed to improve the perception and treatment of atherogenic dyslipidemia.
ConclusionsThe experts involved in this study were shown to be familiar with the concept and the importance of atherogenic dyslipidemia. The few situations in which a consensus could not be found were mainly related to the interpretation and/or relevance of the available evidence.
American Association of Clinical Endocrinologists
Action to Control Cardiovascular Risk in Diabetes
American College of Endocrinology
Latin American Academy for the Study of Lipids
acidente vascular cerebral
Colesterol de lipoproteínas de alta densidade
Colesterol de lipoproteínas de baixa densidade
Consenso Dislipidemia Aterogénica Portugal
Cardiovascular
Doenc¸a cardiovascular
Diabetes mellitus
Dyslipidemia International Study
European Atherosclerosis Society
Agência Europeia para o Medicamento
European Society of Cardiology
European Study on Cardiovascular Risk Prevention and Management in Usual Daily Practice
Enofibrate Intervention and Event Lowering in Diabetes
Lipoproteínas de alta densidade
International Atherosclerosis Society
Lipoproteínas de baixa densidade
The National Institute for Health and Care Excellence
National Lipid Association
Organizac¸ão Mundial de Saúde
Pressão arterial
Proproteína convertase subtilisina‐kexina tipo 9
Residual Risk Reduction Initiative
Sociedad Espãnola de Arteriosclerosis
Triglicerídeos
Lipoproteínas de muito baixa densidade
De acordo com a Organização para a Cooperação e Desenvolvimento Económico (OCDE), e apesar da diminuição substancial verificada nas últimas décadas, as doenças cardiovasculares (DCV) permanecem como a primeira causa de morte na maioria dos países da OCDE, representando mais de um terço (36%) de todas as mortes em 20151. Em Portugal, durante o ano de 2016, as doenças do aparelho circulatório foram responsáveis por 32 805 óbitos (29,6% da mortalidade). O número de anos potenciais de vida perdidos foi de 47 923 anos, o que corresponde a uma taxa de 546,6 por 100 mil habitantes e a um número médio de anos de vida perdidos de 10,82.
Os fatores de risco associados à DCV são amplamente conhecidos e incluem a idade, o género, a etnia, a, história familiar, os hábitos tabágicos, as dislipidemias, a hipertensão arterial, a diabetes mellitus (DM), a obesidade e o sedentarismo3,4. Alguns destes fatores de risco são modificáveis e podem ser controlados com recurso a alterações no estilo de vida e terapêutica farmacológica adequada. Não obstante, em determinadas situações persiste um risco de DCV designado como «residual», definido como o risco que permanece depois de alcançados os objetivos terapêuticos para o colesterol de lipoproteínas de baixa densidade (c‐LDL), pressão arterial e glicemia5.
A dislipidemia aterogénica – caracterizada por uma elevação dos níveis de triglicerídeos (TG), lipoproteínas de muito baixa densidade (VLDL), partículas de LDL pequenas e densas e por uma redução dos níveis das lipoproteínas de alta densidade (HDL) – contribui, de forma significativa, para o risco CV residual5. De facto, vários estudos têm vindo a demonstrar que o desequilíbrio provocado pela elevação de TG (partículas pró‐aterogénicas, especialmente quando enriquecidas em colesterol nas remanescentes) e redução de c‐HDL aumenta o risco de DCV independentemente dos níveis de c‐LDL6,7. Assim, a deteção e o tratamento da dislipidemia aterogénica assumem hoje um papel relevante no controlo do risco CV residual, particularmente em indivíduos em que esta forma de dislipidemia é relativamente prevalente (como sendo o caso de doentes com síndrome metabólica e/ou obesidade e diabetes).
Em termos epidemiológicos, a dislipidemia aterogénica apresenta uma prevalência preocupante. O estudo Eurika8 (European Study on Cardiovascular Risk Prevention and Management in Usual Daily Practice) envolveu 7641 doentes sem história clínica de DCV, mas com pelo menos um fator de risco. Destes, 20,8% tinham níveis de TG elevados (≥ 2,3 mmol/l ou 200mg/dl), 22,1% tinham redução dos níveis de c‐HDL (< 1,0 mmol/l ou 40mg/dl nos homens e < 1,3 mmol/l ou 50mg/dl nas mulheres) e 9,9% apresentavam ambas as condições simultaneamente8. Não obstante, cerca de 55% destes doentes não estavam a fazer qualquer tratamento antidislipidémico. O estudo DYSIS (Dyslipidemia International Study), por outro lado, avaliou a prevalência de alterações lipídicas em doentes já medicados com estatinas9. Em Portugal foram incluídos 916 doentes e os resultados mostraram que 39,2% tinham níveis de TG elevados (> 1,7 mmol/l ou 150mg/dl) e 22,2% tinham níveis de c‐HDL reduzidos (< 1,0 mmol/l ou 40mg/dl nos homens e <1,2 mmol/l ou 46mg/dl nas mulheres)10. Já numa fase posterior e a nível internacional, o estudo DYSIS II incluiu 10 661 doentes com doença coronária estável ou síndrome coronária aguda11. Dos que tinham prescrita terapêutica antidislipidémica, a mediana e os intervalos interquartil (IQR) dos níveis de c‐HDL situavam‐se nos 42,0 mg/dl (35,0‐51,0) e 39,0 mg/dl (33,0‐47,0), enquanto que os de TG estavam nos 120,0 mg/dl (89,0 – 164,0) e 127,0 mg/dl (94,0 ‐ 177,0), respetivamente11. Estes resultados, no seu conjunto, apontam para uma frequência elevada de alterações lipídicas consistentes com o fenótipo da dislipidemia aterogénica, sugerindo que esta patologia se encontra subdiagnosticada e submedicada. Tendo em consideração a sua relevância no risco CV residual, urge investir na educação e informação dos profissionais de saúde de forma a melhorar a deteção, monitoração e tratamento desta forma de dislipidemia.
Este estudo, designado CODAP (Consenso Dislipidemia Aterogénica Portugal), teve como principais objetivos: i) analisar a opinião dos peritos portugueses e gerar um consenso relativamente à definição, ao diagnóstico e à melhor terapêutica para doentes com dislipidemia aterogénica; ii) contribuir para uma uniformização da prática clínica neste contexto.
MétodosDesenho do estudoEste estudo consistiu na aplicação de um questionário a um grupo de especialistas seguindo uma metodologia Delphi adaptada12,13. De forma breve, esta metodologia envolve o desenvolvimento de um inquérito por parte de uma comissão científica, inquérito esse que é posteriormente distribuído a um painel de especialistas previamente convidados a participar no estudo. As respostas obtidas inicialmente (primeira volta) são analisadas pela comissão científica, sendo que as questões para as quais não se verificar consenso podem ser alteradas e reenviadas ao painel científico (juntamente com os resultados da primeira volta) solicitando nova resposta. Este processo é repetido até à obtenção de uma percentagem de consenso considerada satisfatória.
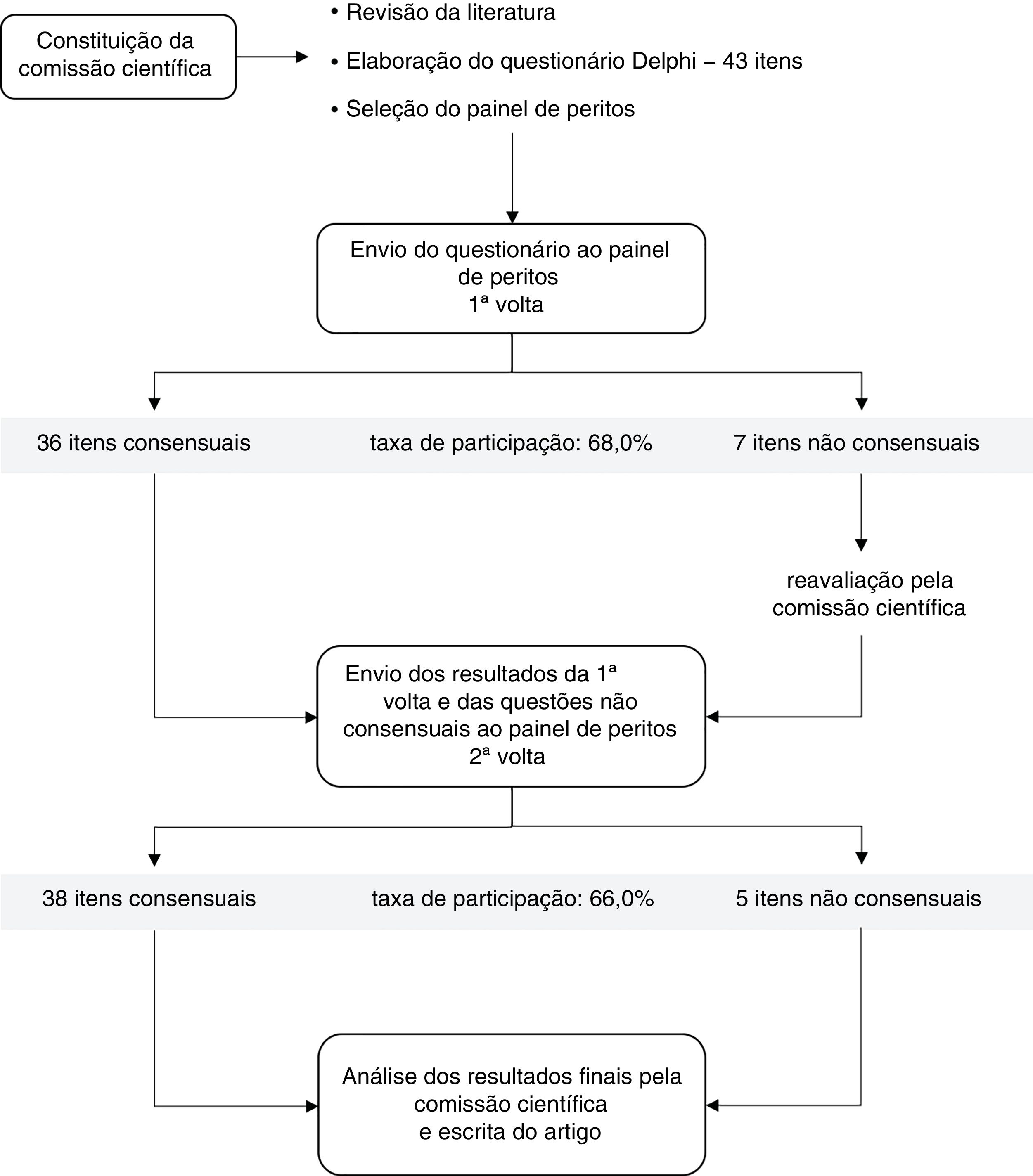
Este estudo desenvolveu‐se em quatro etapas diferentes (figura 1): 1) formação de uma comissão científica e elaboração de um questionário sobre vários aspetos da dislipidemia aterogénica; 2) escolha e convite de membros para o painel de especialistas, constituído por médicos especialistas de diferentes áreas; 3) resposta ao inquérito por parte do painel de especialistas (em duas voltas); e 4) análise e discussão dos resultados finais por parte da comissão científica. Os convites para o painel de especialistas foram feitos de forma a assegurar a maior representatividade possível dos médicos envolvidos na deteção e no tratamento da dislipidemia aterogénica, tendo sido incluídas quatro especialidades diferentes: cardiologia, medicina interna, medicina geral e familiar e endocrinologia. Os médicos convidados foram cuidadosamente selecionados a partir da listagem dos sócios da Sociedade Portuguesa de Aterosclerose ou outras sociedades científicas pertinentes, sendo todos eles médicos especialistas de reconhecida competência sobre o tema abordado. Para garantir uma representatividade idêntica de todas as especialidades, um número semelhante de convites (10‐12) foi enviado para cada grupo, com exceção da endocrinologia (que incluiu um subgrupo de médicos com particular interesse na diabetologia, totalizando 17 convites). O questionário foi colocado numa plataforma online e as respostas foram recolhidas por via eletrónica.
Criação do questionário e definição de consensoO questionário inicial incluiu 43 afirmações sobre diferentes aspetos da dislipidemia aterogénica: três diziam respeito à definição do conceito, três a aspetos de epidemiologia, sete ao impacto da dislipidemia aterogénica no risco de DCV, oito a métodos de deteção e diagnóstico, sete a objetivos terapêuticos e 15 ao tratamento. Estes itens foram avaliados pelos membros do painel de acordo com uma escala tipo Likert de 1 a 9 (1, discordo totalmente; 9, concordo totalmente), em que cada opção podia ser fundamentada pelos membros do painel através do preenchimento de um campo livre no questionário. Foi considerado que existia consenso sempre que se verificavam simultaneamente as seguintes condições: 1) a mediana das respostas dos membros do painel situava‐se no intervalo 1 a 3 (consenso em desacordo) ou 7 a 9 (consenso em acordo); 2) o intervalo interquartil da mediana era igual ou inferior a 4; 3) o número de membros do painel que votaram fora do intervalo de consenso (1 a 3 ou 7 a 9) era inferior a um terço (33,33%) dos votos totais.
ResultadosNuma fase inicial, 50 médicos foram convidados a participar no estudo: 12 especialistas em cardiologia, 11 em medicina interna, 10 em medicina geral e familiar e 17 em endocrinologia. Na primeira volta obtiveram‐se 34 respostas, o que corresponde a uma taxa de participação de 68,0% (figura 1). As taxas de participação por especialidade foram as seguintes: 58,3% em cardiologia, 90,9% em medicina interna, 80,0% em medicina geral e familiar e 52,9% em endocrinologia. Após a segunda (e última) volta do questionário obtiveram‐se 33 respostas, o que corresponde a uma taxa de participação final de 66,0% (figura 1). O membro do painel que não respondeu à segunda volta pertencia à especialidade de cardiologia, que teve assim uma taxa de participação final de 50,0%.
Trinta e seis (83,7%) dos 43 itens colocados à consideração foram consensuais (em concordância) após a primeira volta do questionário (figura 1 e tabela 1). Dos sete itens não consensuais, três foram reformulados e quatro foram mantidos tal como estavam, sendo que para dois deles foi expressamente solicitado aos membros do painel uma justificação para a sua opção. Após a segunda volta, dois dos sete itens não consensuais obtiveram anuência (tabela 1): itens III.1 e VI.15. A percentagem de consenso final foi então de 88,4% (figura 1. e tabela 1), sendo que para cinco itens não foi encontrado consenso: III.3, IV.7, V.I, VI.9 e VI.14.
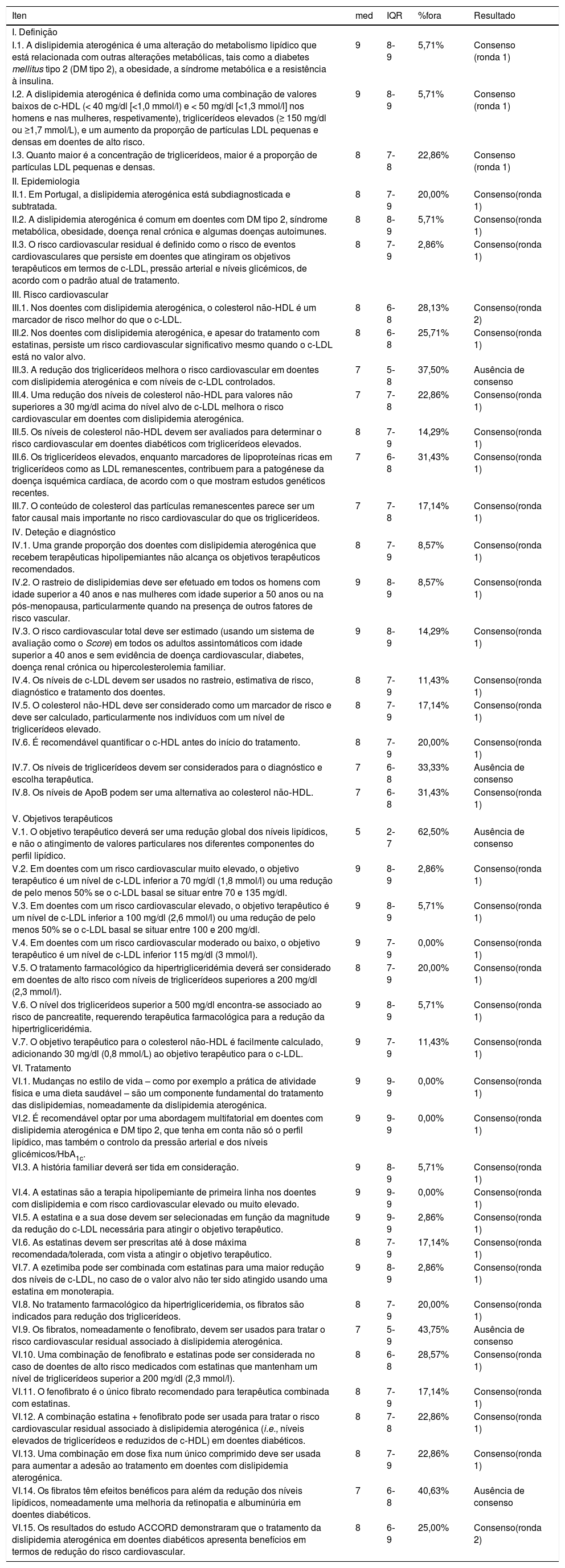
Resultados do questionário Delphi
| Iten | med | IQR | %fora | Resultado |
|---|---|---|---|---|
| I. Definição | ||||
| I.1. A dislipidemia aterogénica é uma alteração do metabolismo lipídico que está relacionada com outras alterações metabólicas, tais como a diabetes mellitus tipo 2 (DM tipo 2), a obesidade, a síndrome metabólica e a resistência à insulina. | 9 | 8‐9 | 5,71% | Consenso (ronda 1) |
| I.2. A dislipidemia aterogénica é definida como uma combinação de valores baixos de c‐HDL (< 40 mg/dl [<1,0 mmol/l) e < 50 mg/dl [<1,3 mmol/l] nos homens e nas mulheres, respetivamente), triglicerídeos elevados (≥ 150 mg/dl ou ≥1,7 mmol/L), e um aumento da proporção de partículas LDL pequenas e densas em doentes de alto risco. | 9 | 8‐9 | 5,71% | Consenso (ronda 1) |
| I.3. Quanto maior é a concentração de triglicerídeos, maior é a proporção de partículas LDL pequenas e densas. | 8 | 7‐8 | 22,86% | Consenso (ronda 1) |
| II. Epidemiologia | ||||
| II.1. Em Portugal, a dislipidemia aterogénica está subdiagnosticada e subtratada. | 8 | 7‐9 | 20,00% | Consenso(ronda 1) |
| II.2. A dislipidemia aterogénica é comum em doentes com DM tipo 2, síndrome metabólica, obesidade, doença renal crónica e algumas doenças autoimunes. | 8 | 8‐9 | 5,71% | Consenso(ronda 1) |
| II.3. O risco cardiovascular residual é definido como o risco de eventos cardiovasculares que persiste em doentes que atingiram os objetivos terapêuticos em termos de c‐LDL, pressão arterial e níveis glicémicos, de acordo com o padrão atual de tratamento. | 8 | 7‐9 | 2,86% | Consenso(ronda 1) |
| III. Risco cardiovascular | ||||
| III.1. Nos doentes com dislipidemia aterogénica, o colesterol não‐HDL é um marcador de risco melhor do que o c‐LDL. | 8 | 6‐8 | 28,13% | Consenso(ronda 2) |
| III.2. Nos doentes com dislipidemia aterogénica, e apesar do tratamento com estatinas, persiste um risco cardiovascular significativo mesmo quando o c‐LDL está no valor alvo. | 8 | 6‐8 | 25,71% | Consenso(ronda 1) |
| III.3. A redução dos triglicerídeos melhora o risco cardiovascular em doentes com dislipidemia aterogénica e com níveis de c‐LDL controlados. | 7 | 5‐8 | 37,50% | Ausência de consenso |
| III.4. Uma redução dos níveis de colesterol não‐HDL para valores não superiores a 30 mg/dl acima do nível alvo de c‐LDL melhora o risco cardiovascular em doentes com dislipidemia aterogénica. | 7 | 7‐8 | 22,86% | Consenso(ronda 1) |
| III.5. Os níveis de colesterol não‐HDL devem ser avaliados para determinar o risco cardiovascular em doentes diabéticos com triglicerídeos elevados. | 8 | 7‐9 | 14,29% | Consenso(ronda 1) |
| III.6. Os triglicerídeos elevados, enquanto marcadores de lipoproteínas ricas em triglicerídeos como as LDL remanescentes, contribuem para a patogénese da doença isquémica cardíaca, de acordo com o que mostram estudos genéticos recentes. | 7 | 6‐8 | 31,43% | Consenso(ronda 1) |
| III.7. O conteúdo de colesterol das partículas remanescentes parece ser um fator causal mais importante no risco cardiovascular do que os triglicerídeos. | 7 | 7‐8 | 17,14% | Consenso(ronda 1) |
| IV. Deteção e diagnóstico | ||||
| IV.1. Uma grande proporção dos doentes com dislipidemia aterogénica que recebem terapêuticas hipolipemiantes não alcança os objetivos terapêuticos recomendados. | 8 | 7‐9 | 8,57% | Consenso(ronda 1) |
| IV.2. O rastreio de dislipidemias deve ser efetuado em todos os homens com idade superior a 40 anos e nas mulheres com idade superior a 50 anos ou na pós‐menopausa, particularmente quando na presença de outros fatores de risco vascular. | 9 | 8‐9 | 8,57% | Consenso(ronda 1) |
| IV.3. O risco cardiovascular total deve ser estimado (usando um sistema de avaliação como o Score) em todos os adultos assintomáticos com idade superior a 40 anos e sem evidência de doença cardiovascular, diabetes, doença renal crónica ou hipercolesterolemia familiar. | 9 | 8‐9 | 14,29% | Consenso(ronda 1) |
| IV.4. Os níveis de c‐LDL devem ser usados no rastreio, estimativa de risco, diagnóstico e tratamento dos doentes. | 8 | 7‐9 | 11,43% | Consenso(ronda 1) |
| IV.5. O colesterol não‐HDL deve ser considerado como um marcador de risco e deve ser calculado, particularmente nos indivíduos com um nível de triglicerídeos elevado. | 8 | 7‐9 | 17,14% | Consenso(ronda 1) |
| IV.6. É recomendável quantificar o c‐HDL antes do início do tratamento. | 8 | 7‐9 | 20,00% | Consenso(ronda 1) |
| IV.7. Os níveis de triglicerídeos devem ser considerados para o diagnóstico e escolha terapêutica. | 7 | 6‐8 | 33,33% | Ausência de consenso |
| IV.8. Os níveis de ApoB podem ser uma alternativa ao colesterol não‐HDL. | 7 | 6‐8 | 31,43% | Consenso(ronda 1) |
| V. Objetivos terapêuticos | ||||
| V.1. O objetivo terapêutico deverá ser uma redução global dos níveis lipídicos, e não o atingimento de valores particulares nos diferentes componentes do perfil lipídico. | 5 | 2‐7 | 62,50% | Ausência de consenso |
| V.2. Em doentes com um risco cardiovascular muito elevado, o objetivo terapêutico é um nível de c‐LDL inferior a 70 mg/dl (1,8 mmol/l) ou uma redução de pelo menos 50% se o c‐LDL basal se situar entre 70 e 135 mg/dl. | 9 | 8‐9 | 2,86% | Consenso(ronda 1) |
| V.3. Em doentes com um risco cardiovascular elevado, o objetivo terapêutico é um nível de c‐LDL inferior a 100 mg/dl (2,6 mmol/l) ou uma redução de pelo menos 50% se o c‐LDL basal se situar entre 100 e 200 mg/dl. | 9 | 8‐9 | 5,71% | Consenso(ronda 1) |
| V.4. Em doentes com um risco cardiovascular moderado ou baixo, o objetivo terapêutico é um nível de c‐LDL inferior 115 mg/dl (3 mmol/l). | 9 | 7‐9 | 0,00% | Consenso(ronda 1) |
| V.5. O tratamento farmacológico da hipertrigliceridémia deverá ser considerado em doentes de alto risco com níveis de triglicerídeos superiores a 200 mg/dl (2,3 mmol/l). | 8 | 7‐9 | 20,00% | Consenso(ronda 1) |
| V.6. O nível dos triglicerídeos superior a 500 mg/dl encontra‐se associado ao risco de pancreatite, requerendo terapêutica farmacológica para a redução da hipertrigliceridémia. | 9 | 8‐9 | 5,71% | Consenso(ronda 1) |
| V.7. O objetivo terapêutico para o colesterol não‐HDL é facilmente calculado, adicionando 30 mg/dl (0,8 mmol/L) ao objetivo terapêutico para o c‐LDL. | 9 | 7‐9 | 11,43% | Consenso(ronda 1) |
| VI. Tratamento | ||||
| VI.1. Mudanças no estilo de vida – como por exemplo a prática de atividade física e uma dieta saudável – são um componente fundamental do tratamento das dislipidemias, nomeadamente da dislipidemia aterogénica. | 9 | 9‐9 | 0,00% | Consenso(ronda 1) |
| VI.2. É recomendável optar por uma abordagem multifatorial em doentes com dislipidemia aterogénica e DM tipo 2, que tenha em conta não só o perfil lipídico, mas também o controlo da pressão arterial e dos níveis glicémicos/HbA1c. | 9 | 9‐9 | 0,00% | Consenso(ronda 1) |
| VI.3. A história familiar deverá ser tida em consideração. | 9 | 8‐9 | 5,71% | Consenso(ronda 1) |
| VI.4. A estatinas são a terapia hipolipemiante de primeira linha nos doentes com dislipidemia e com risco cardiovascular elevado ou muito elevado. | 9 | 9‐9 | 0,00% | Consenso(ronda 1) |
| VI.5. A estatina e a sua dose devem ser selecionadas em função da magnitude da redução do c‐LDL necessária para atingir o objetivo terapêutico. | 9 | 9‐9 | 2,86% | Consenso(ronda 1) |
| VI.6. As estatinas devem ser prescritas até à dose máxima recomendada/tolerada, com vista a atingir o objetivo terapêutico. | 8 | 7‐9 | 17,14% | Consenso(ronda 1) |
| VI.7. A ezetimiba pode ser combinada com estatinas para uma maior redução dos níveis de c‐LDL, no caso de o valor alvo não ter sido atingido usando uma estatina em monoterapia. | 9 | 8‐9 | 2,86% | Consenso(ronda 1) |
| VI.8. No tratamento farmacológico da hipertrigliceridemia, os fibratos são indicados para redução dos triglicerídeos. | 8 | 7‐9 | 20,00% | Consenso(ronda 1) |
| VI.9. Os fibratos, nomeadamente o fenofibrato, devem ser usados para tratar o risco cardiovascular residual associado à dislipidemia aterogénica. | 7 | 5‐9 | 43,75% | Ausência de consenso |
| VI.10. Uma combinação de fenofibrato e estatinas pode ser considerada no caso de doentes de alto risco medicados com estatinas que mantenham um nível de triglicerídeos superior a 200 mg/dl (2,3 mmol/l). | 8 | 6‐8 | 28,57% | Consenso(ronda 1) |
| VI.11. O fenofibrato é o único fibrato recomendado para terapêutica combinada com estatinas. | 8 | 7‐9 | 17,14% | Consenso(ronda 1) |
| VI.12. A combinação estatina + fenofibrato pode ser usada para tratar o risco cardiovascular residual associado à dislipidemia aterogénica (i.e., níveis elevados de triglicerídeos e reduzidos de c‐HDL) em doentes diabéticos. | 8 | 7‐8 | 22,86% | Consenso(ronda 1) |
| VI.13. Uma combinação em dose fixa num único comprimido deve ser usada para aumentar a adesão ao tratamento em doentes com dislipidemia aterogénica. | 8 | 7‐9 | 22,86% | Consenso(ronda 1) |
| VI.14. Os fibratos têm efeitos benéficos para além da redução dos níveis lipídicos, nomeadamente uma melhoria da retinopatia e albuminúria em doentes diabéticos. | 7 | 6‐8 | 40,63% | Ausência de consenso |
| VI.15. Os resultados do estudo ACCORD demonstraram que o tratamento da dislipidemia aterogénica em doentes diabéticos apresenta benefícios em termos de redução do risco cardiovascular. | 8 | 6‐9 | 25,00% | Consenso(ronda 2) |
%fora, % de votos fora do intervalo 1‐3, 4‐6 ou 7‐9 (de acordo com a localização da mediana); IQR, intervalo interquartil; Med, mediana.
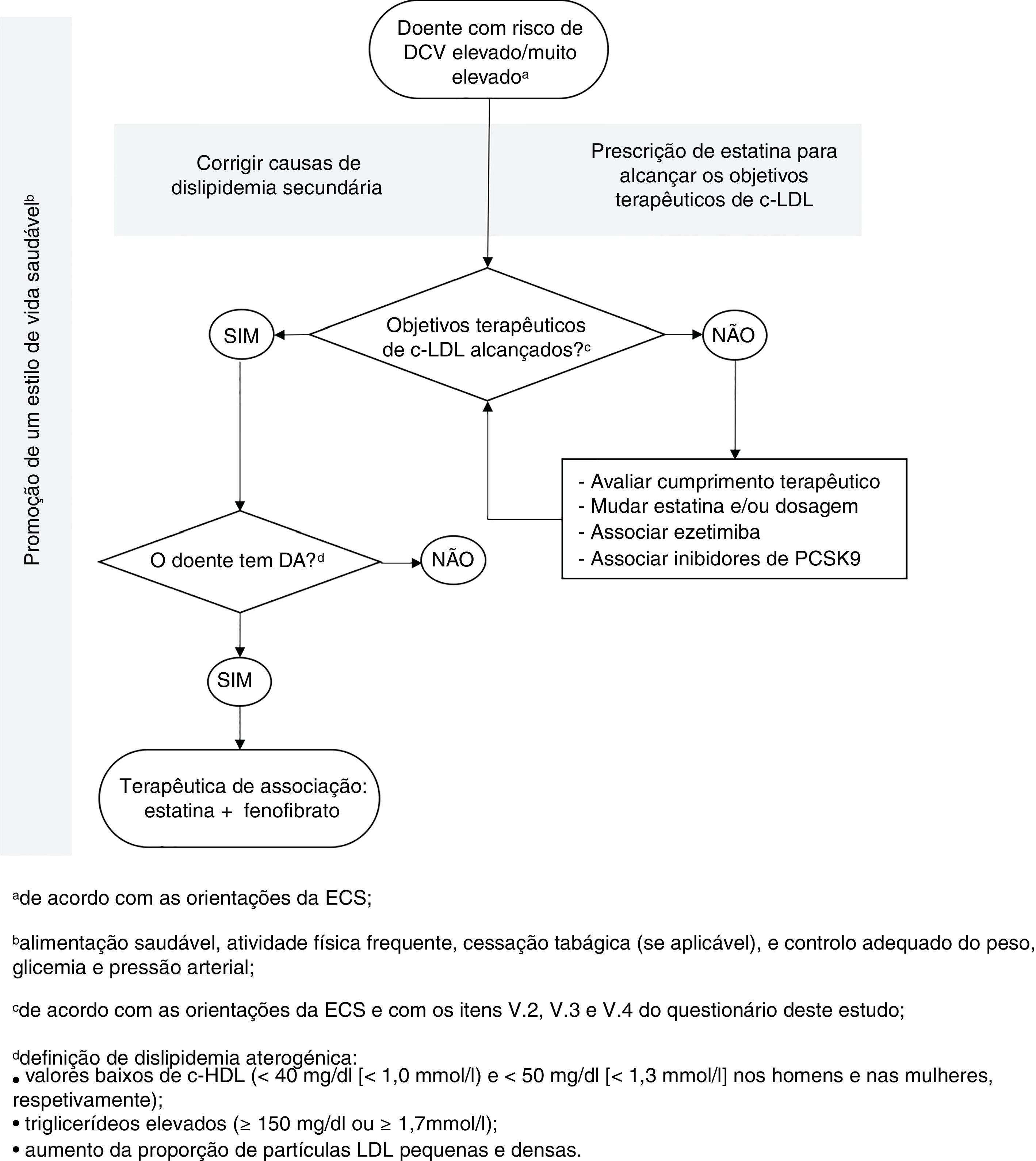
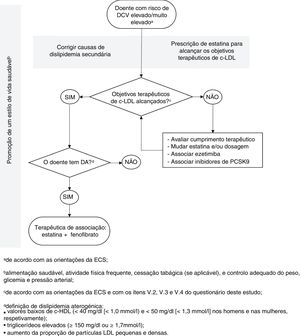
Tendo como base a informação presente na literatura e as respostas obtidas no questionário, e com vista a uniformizar a prática clínica no contexto da dislipidemia aterogénica, a comissão científica elaborou um algoritmo de tratamento para doentes com risco de eventos CV elevado ou muito elevado (figura 2). Este algoritmo considera que, após normalização dos níveis de c‐LDL num doente medicado com estatina e com um estilo de vida saudável, a possibilidade de dislipidemia aterogénica deve ser avaliada. Em caso de confirmação desta patologia, a comissão científica considera que a melhor terapêutica disponível atualmente consiste na associação do fenofibrato à estatina.
Algoritmo para tratamento de doentes com dislipidemia aterogénica. c‐LDL, colesterol de lipoproteínas de baixa densidade; c‐HDL, colesterol de lipoproteínas de alta densidade; DA, dislipidemia aterogénica; DCV, doença cardiovascular; PCSK9, proproteína convertase subtilisina‐kexina tipo 9.
Este estudo revelou que a opinião dos especialistas portugueses sobre a definição, importância, diagnóstico e tratamento da dislipidemia aterogénica é, em grande parte, consensual, sendo que se verificou concordância entre os peritos em 88,4% dos itens. Este valor foi semelhante ao reportado num estudo análogo feito em Espanha, em que se obteve uma taxa de consenso de 87,4%14. No entanto, a participação foi inferior ao expectável, tendo‐se obtido respostas apenas a 66% dos convites enviados (após as duas voltas). Se, numa fase inicial, se procurou que os membros do painel estivessem distribuídos de forma homogénea pelas especialidades com maior experiência e vivência clínica relativamente ao problema abordado – cardiologia, medicina interna, medicina geral e familiar e endocrinologia (esta última especialidade incluindo um subgrupo de médicos particularmente interessados em diabetologia) – no fim verificou‐se que algumas especialidades tiveram uma representatividade claramente superior. Esta limitação não é específica deste estudo, mas é antes uma questão inerente a qualquer metodologia que assente na análise de respostas a um questionário: é impossível garantir, à partida, um determinado número de respostas ou a sua distribuição na população. Não obstante, consideramos que as repostas obtidas são representativas de um grupo de médicos com interesse no tema – independentemente da sua especialidade – e que a sua análise e divulgação cumpre os objetivos iniciais.
Dentro dos tópicos consensuais, destacam‐se os relativos à definição e epidemiologia da dislipidemia aterogénica, os únicos em que foi obtido consenso para todos os itens. A definição analítica de dislipidemia aterogénica, descrita como uma combinação de valores baixos de c‐HDL (< 40mg/dl [< 1,0 mmol/l) e < 50mg/dl [< 1,3 mmol/l] nos homens e nas mulheres, respetivamente), TG elevados (≥ 150mg/dl ou ≥ 1,7 mmol/l), e um aumento da proporção de partículas LDL pequenas e densas em doentes de alto risco, foi consensual e teve o acordo (votação na zona 7 a 9) de 94,3% dos membros do painel. Esta definição é globalmente aceite na literatura atual e foi a usada num artigo recente de consenso que reuniu especialistas europeus em DCV5,15. Não obstante, é importante referir que os valores usados nesta definição podem variar: a título de exemplo, a SEA (Sociedad Española de Arteriosclerosis) e um grupo de especialistas europeus publicaram recentemente dois artigos em que foi assumido um limite de 200mg/dl (2,3 mmol/l) para os TG16,17. Relativamente à epidemiologia, e também de acordo com a evidência científica e epidemiológica disponível, o painel foi consensual no reconhecimento de que a dislipidemia aterogénica é particularmente prevalente em doentes com obesidade, síndrome metabólica, DM tipo 2 e outras alterações metabólicas ou doenças autoimunes5,17. Para além disso, 80% dos inquiridos concordaram (votação na zona 7 a 9) que a dislipidemia aterogénica está subdiagnosticada e subtratada, algo que tem vindo a ser reconhecido em diferentes estudos e que parece ser uma realidade a nível global8,10,18.
A importância dos níveis de c‐LDL no rastreio, na estimativa de risco CV, no diagnóstico e tratamento dos doentes foi consensual para o painel de inquiridos. Foi também consensual a aceitação de objetivos terapêuticos de c‐LDL personalizados de acordo com o nível de risco do doente, tal como preconizado nas linhas orientadoras da prática clínica publicadas em conjunto pela European Society of Cardiology (ESC) e pela European Atherosclerosis Society (EAS), entre outras19. No entanto, e não obstante a incontornável importância dos níveis de c‐LDL neste contexto, o painel reconheceu a existência de um risco residual que persiste após serem atingidos os objetivos terapêuticos relativos a esta fração lipídica. Esta perceção vai de encontro à que é sustentada pela Residual Risk Reduction Initiative (R3i), que recentemente reviu a sua primeira publicação e realçou, apoiada por uma extensa revisão da literatura, o papel preponderante do desequilíbrio causado pela elevação dos TG e redução do c‐HDL no risco residual de DCV6,20. De facto, mesmo a terapêutica médica otimizada incluindo inibidores de PCSK9 (proproteína convertase subtilisina‐kexina tipo 9), novos fármacos capazes de reduzir significativamente os níveis de c‐LDL21, parece ser incapaz de eliminar o risco CV na sua totalidade.
Em conformidade com o reconhecimento do risco residual, o painel identificou o colesterol não‐HDL como um importante marcador de risco de DCV. De facto, 71,9% dos elementos inquiridos consideraram (votação na zona 7 a 9) que o colesterol não‐HDL é um marcador de risco melhor do que o c‐LDL em doentes com dislipidemia aterogénica. Esta visão é amplamente suportada pela literatura: o colesterol não‐HDL, sendo o somatório do c‐LDL e do colesterol remanescente (constituído pelo c‐VLDL e pelo c‐IDL [lipoproteínas de densidade intermédia]), representa a fração aterogénica do colesterol de uma forma mais abrangente do que o c‐LDL15,22–24. Tal tem vindo a ser progressivamente reconhecido pela comunidade médica internacional, sendo que o colesterol não‐HDL começa a assumir um papel importante nas linhas de orientação da prática clínica: enquanto a ESC/EAS, a International Atherosclerosis Society (IAS) e a Sociedade Canadiana de DCV definem o colesterol não‐HDL como um objetivo terapêutico «secundário» ou «alternativo» ao c‐LDL19,25,26, a National Lipid Association (NLA) e a publicação conjunta da American Association of Clinical Endocrinologists (AACE) e da American College of Endocrinology (ACE) estabelecem objetivos paralelos para o c‐LDL e para o colesterol não‐HDL27,28 e a National Institute for Health and Care Excelence (NICE) estabelece o colesterol não‐HDL como único objetivo terapêutico29. No mesmo sentido, um consenso recente das Sociedades Científicas Portuguesas sustenta que o colesterol não‐HDL deve ser ponderado como um indicador superior de risco na abordagem clínica da dislipidemia e como um objetivo terapêutico secundário a ser almejado, particularmente em certas situações clínicas (e.g. presença de hipertrigliceridemia) 30. É também de referir neste contexto que o painel considerou que os níveis de ApoB podem ser uma alternativa ao colesterol não‐HDL. Muito embora não sendo idênticos, os níveis de colesterol não‐HDL estão intrinsecamente relacionados com os de ApoB, o que justifica a perceção desta equivalência e o facto de muitas das linhas orientadoras acima referidas apontarem também objetivos terapêuticos para a ApoB. No entanto, o facto de o colesterol não‐HDL ser facilmente determinado e reconhecido por todos os profissionais de saúde torna‐o um objetivo terapêutico mais atrativo.
Curiosamente, a importância dos TG no risco de DCV não foi consensual entre os membros do painel. De facto, e durante várias décadas, era assumido que os TG não desempenhavam um papel relevante no desenvolvimento da DCV. No entanto, estudos recentes vieram a demonstrar que concentrações elevadas de TG e colesterol remanescente contribuem diretamente para a fisiopatologia da doença isquémica cardíaca31,32. Sabe‐se hoje que TG entre os 200 e os 600mg/dl (2,3 a 6,8 mmol/l) indica acumulação de partículas de colesterol remanescentes ricas em TG que são altamente aterogénicas33,34. De referir ainda que existem três ensaios clínicos que estão a analisar a incidência de DCV em doentes com hipertrigliceridemia no sentido de confirmar que níveis elevados de TG contribuem de forma significativa para o risco residual de DCV: em dois deles estão a ser usados ácidos gordos ómega‐3 (formulações de ácidos carboxílicos ou ésteres etílicos de ácido eicosapentanóico puro)35,36, enquanto no terceiro está a ser usado um novo fibrato (pemafibrato) 37.
É importante notar que, ao reconhecer a importância do colesterol não‐HDL, o painel reconhece, de alguma forma, a relevância dos TG, já que a concentração dos últimos está intrinsecamente relacionada com a concentração de c‐VLDL e c‐IDL. Da mesma forma, o painel não foi consensual no que diz respeito à valorização dos níveis de TG no diagnóstico e escolha terapêutica, mas concordou com a necessidade de tratar a hipertrigliceridemia (valores superiores a 200mg/dl [2,3 mmol/l]) em doentes de alto risco, tal como é recomendado pelas linhas de orientação da prática clínica da ESC/EAS19. Isto sugere que a falta de consenso nas questões relacionadas com os TG poderá estar relacionada não com uma ausência de valorização desta fração lipídica, mas antes com as várias considerações (e limitações) inerentes à sua quantificação30,38. De facto, é sabido que os valores de TG apresentam uma variação intraindividual não desprezível, o que pode colocar dificuldades à sua interpretação. Uma questão recorrente é se a sua medição deve ser feita em jejum ou no período pós‐prandial, com dados recentes a confirmar que os níveis de TG após refeições podem conter informações suplementares sobre o colesterol remanescente, sendo, portanto, uma medição complementar à dos TG em jejum30. Seja como for, e neste contexto, os especialistas tenderão a favorecer o colesterol não‐HDL, que é de fácil determinação e cujo valor providencia uma medida indireta dos TG. É também possível que a evidência científica atualmente disponível não seja suficientemente robusta para convencer uma proporção considerável dos especialistas sobre a importância dos TG. Neste contexto, é interessante notar que o papel destas partículas lipídicas como fator de risco independente para a DCV também não foi consensual no estudo sobre a dislipidemia aterogénica feito junto de especialistas espanhóis14.
Um outro ponto não consensual foi o V.I: o painel não concordou nem discordou com a afirmação de que o objetivo terapêutico deverá ser uma redução global dos níveis lipídicos, por oposição ao atingimento de valores particulares nos diferentes componentes do perfil lipídico. A ausência de consenso neste ponto poderá ter diferentes interpretações. Por um lado, pode demonstrar o reconhecimento do significado da fração de c‐HDL, cujo valor está inversamente relacionado com o risco de DCV39. Por outro lado, pode também estar relacionada com uma questão mais conceptual, que se prende com o facto de o objetivo da terapia ser reduzir o risco CV (e não reduzir a presença dos marcadores de risco). De facto, mesmo nas linhas de orientação da prática clínica que estabelecem valores alvo de c‐LDL ou de colesterol não‐HDL, estes valores são geralmente objetivados em função do risco de cada doente19,27,28. Estas questões poderão ter levantado algumas dúvidas na interpretação deste item, justificando a dispersão de votos e a consequente ausência de consenso.
No que se refere ao tratamento, o painel foi unânime no reconhecimento da importância de um estilo de vida saudável no tratamento das dislipidemias, bem como na escolha das estatinas como fármacos de primeira linha para o tratamento destas patologias em doentes com risco de DCV elevado ou muito elevado e a adição de ezetimiba à terapia de indivíduos que não alcançaram o objetivo terapêutico de c‐LDL. Estes itens vão de encontro à generalidade do que é recomendado na maioria das linhas de orientação de prática clínica19,25–29.
A utilização de fibratos na terapêutica da dislipidemia aterogénica também foi, de forma geral, consensual. De facto, o painel reconheceu que os fibratos são indicados para a redução dos TG e que a associação de fenofibrato às estatinas pode ser considerada para tratar a hipertrigliceridemia em indivíduos de alto risco, bem como o RCV residual associado à dislipidemia aterogénica em indivíduos diabéticos. De referir que o fenofibrato apresenta um risco baixo de interações medicamentosas (sendo um fraco inibidor da CYP2C19 e da CYP2A6 e, em concentrações terapêuticas, um inibidor discreto da CYP2C9), bem como uma interferência reduzida na glucuronidação das estatinas e um perfil de segurança comprovado em estudos de intervenção. No entanto, não houve consenso no reconhecimento de que os fibratos (nomeadamente o fenofibrato) devem ser usados para tratar o risco CV residual associado à dislipidemia aterogénica. Esta aparente discrepância sobre o valor terapêutico do fenofibrato no contexto da dislipidemia aterogénica encontra justificação na literatura: os dois principais ensaios aleatorizados que estudaram a eficácia do fenofibrato – o FIELD (Fenofibrate Intervention and Event Lowering in Diabetes) e o ACCORD (Action to Control Cardiovascular Risk in Diabetes) – foram considerados globalmente negativos40,41. De facto, em nenhum deles foi atingida significância estatística relativamente ao objetivo principal (ocorrência de eventos coronários [doença coronária cardíaca fatal ou enfarte do miocárdio não fatal] no FIELD e ocorrência de enfarte do miocárdio não fatal, acidente vascular cerebral [AVC] não fatal ou morte por causas cardiovasculares no ACCORD). Não obstante, alguns resultados secundários do FIELD são claramente favoráveis à utilização de fenofibrato, dos quais se destaca uma redução significativa de 24% em enfartes do miocárdio não fatais e uma redução também significativa de 11% no número total de eventos cardiovasculares41–45. Acresce que a percentagem de indivíduos que iniciou tratamento com outros fármacos antidislipidémicos (e.g. estatinas) foi superior no grupo tratado com placebo (17% versus 8% no grupo tratado com fenofibrato, p < 0,0001), o que poderá ter disfarçado o efeito benéfico do fármaco experimental. Já no ACCORD, uma análise de um subgrupo de indivíduos com níveis de TG superiores a 204mg/dl e níveis de c‐HDL inferiores a 34mg/dl mostrou que o tratamento com fenofibrato esteve associado a uma redução significativa de 31% na incidência de eventos CV43,45,46. É importante referir que esta era uma análise pré‐especificada no protocolo do ACCORD47. Para além disso, uma extensão do seguimento dos doentes envolvidos no ACCORD (designada Accordion) sugeriu um possível efeito legado do fenofibrato: cinco anos após o término do estudo original, os doentes com dislipidemia aterogénica tratados com fenofibrato continuavam a ter um risco de eventos CV significativamente menor do que haviam sido tratados com placebo (HR = 0,73; IC 95% = 0,56‐0,95)48. Finalmente, numa meta‐análise que incluiu o FIELD, o ACCORD e três outros ensaios aleatorizados foi estimado que a utilização de fibratos (versus placebo) diminuía em 30% o risco de eventos CV em indivíduos com dislipidemia aterogénica (p < 0,0001)49. Todos estes resultados demonstram a importância dos fibratos, nomeadamente do fenofibrato, no tratamento de doentes que apresentam um fenótipo consistente com a dislipidemia aterogénica. Como tal, a adição de fibratos ao tratamento destes doentes é já considerada em algumas linhas de orientação da prática clínica, muito embora seja feita de forma cautelosa dada a inexistência de ensaios clínicos aleatorizados especificamente desenvolvidos em populações de doentes com dislipidemia aterogénica15,19,25–27,50.
Surpreendentemente, o painel também não foi consensual relativamente aos efeitos benéficos dos fibratos nas complicações microvasculares dos doentes diabéticos, com apenas 59,4% dos inquiridos a votarem na zona de concordância7–9. No entanto, a evidência científica parece ser clara a este propósito, mostrando que o tratamento com fibratos melhora (ou atrasa o desenvolvimento de) a retinopatia e albuminúria43–46. Este resultado realça a importância da divulgação científica e da formação profissional contínua dos médicos em exercício, de forma a garantir a atualização do conhecimento e adequação das práticas clínicas à melhor evidência científica.
O algoritmo de tratamento proposto pela comissão científica foi baseado na literatura e nas respostas obtidas ao inquérito proposto. De forma geral, este algoritmo é concordante com as linhas de orientação da prática clínica discutidas acima no que diz respeito a: importância de um estilo de vida saudável como base fundamental da terapêutica; utilização de estatinas como fármaco antidislipidémico de primeira linha em indivíduos com risco de DCV elevado ou muito elevado; avaliação dos níveis de c‐LDL como objetivo terapêutico primário; e revisão da terapêutica com estatinas, avaliação da adesão terapêutica e/ou associação de ezetimiba (ou inibidores de PCSK9) quando os objetivos de c‐LDL não são alcançados19,25–28,50. A terapêutica de associação do fenofibrato à estatina é, como foi descrito acima, considerada em algumas linhas de orientação da prática clínica, embora não seja inequivocamente recomendada. Não obstante, a comissão científica considerou que a evidência reunida é já suficiente para justificar a recomendação desta associação terapêutica como a melhor alternativa disponível em situações de indivíduos com risco de DCV elevado ou muito elevado e dislipidemia aterogénica que persiste apesar de tratamento com estatinas40–46,48,49. Para além disso, o fenofibrato é o único fibrato aprovado pela Agência Europeia para o Medicamento (EMA) como um adjuvante da dieta ou outro tratamento/medida não farmacológica para hiperlipidemia mista em doentes com risco cardiovascular elevado, em conjugação com uma estatina, quando os níveis de triglicéridos e de c‐HDL não estão adequadamente controlados. Acresce que, ao contrário do gemfibrozilo, o fenofibrato não apresenta interações significativas com as estatinas, o que parece explicar o menor risco de eventos adversos musculares com a combinação fenofibrato+estatinas (em comparação com a combinação gemfibrozilo+estatinas)19.
O desenho e a aceitação de um algoritmo de tratamento para doentes com dislipidemia aterogénica é essencial para uniformizar a prática clínica e garantir que esta patologia é devidamente identificada e tratada, algo que deverá resultar na redução do risco residual de DCV e, consequentemente, na diminuição da morbilidade e mortalidade associadas. De referir que um artigo de consenso recentemente publicado pela Latin American Academy for the Study of Lipids (Alalip) preconiza um algoritmo muito semelhante para o tratamento de doentes com dislipidemia aterogénica, com a diferença que, para além dos fibratos, considera também a possibilidade de adicionar ácidos gordos ómega‐3 ao tratamento quando o objetivo de colesterol não‐HDL não é atingido18.
ConclusãoOs médicos portugueses que participaram neste estudo mostraram estar familiarizados com a importância da dislipidemia aterogénica no contexto do risco de DCV, particularmente no que diz respeito a: definição de dislipidemia aterogénica e sua associação com outras morbilidades (nomeadamente de natureza metabólica); o facto de a dislipidemia aterogénica ser uma doença subdiagnosticada e, como tal, insuficientemente tratada; a relevância do c‐LDL e colesterol não‐HDL como indicadores de risco e objetivos terapêuticos; a importância de um estilo de vida saudável como elemento fundamental na terapêutica das dislipidemias; o papel das estatinas como terapia antidislipidémica de primeira linha em indivíduos com risco de DCV elevado ou muito elevado; e o reconhecimento de que a associação do fenofibrato às estatinas pode ser usada para tratar o risco CV residual associado à dislipidemia aterogénica em doentes diabéticos. No entanto, e não obstante a evidência disponível na literatura, é notória a existência de alguma incerteza relacionada com o papel desempenhado pelos TG como marcador de risco e na escolha terapêutica, bem como relativamente ao valor terapêutico dos fibratos no tratamento da dislipidemia aterogénica e na prevenção de complicações microvasculares em doentes diabéticos. Enquanto a primeira questão poderá estar relacionada com a maior relevância atribuída ao colesterol não‐HDL quando comparado com os TG, o ceticismo relativamente aos fibratos parece estar essencialmente relacionado com a interpretação e valorização da evidência científica disponível.
Neste contexto, a comissão científica considera fundamental promover a sensibilização para a dislipidemia aterogénica e o risco de DCV associado, bem como a divulgação do conhecimento existente e a implantação de medidas com vista à correta identificação e tratamento adequado desta patologia. Assim, e com base na literatura existente e nas opiniões recolhidas neste estudo, a comissão científica propõe aqui um algoritmo de tratamento no qual se destaca a utilização de estatinas como terapêutica de primeira linha, a avaliação dos níveis de c‐LDL como objetivo de tratamento primário, o despiste do fenótipo de dislipidemia aterogénica e a associação de fenofibrato à terapêutica quando este se verifica. Espera‐se que este algoritmo sirva como ponto de partida para uniformizar e melhorar a prática clínica relativa ao tratamento da dislipidemia aterogénica em Portugal e dessa forma melhorar os índices de morbilidade e mortalidade associados à DCV.
Conflitos de interesseAMS recebeu honorários por palestras ou serviços de consultoria prestados a Amgen, AstraZeneca, Jaba‐Recordati, Merck, Mylan, Novartis e Tecnimede. CA recebeu honorários por serviços prestados a Abbott, Amgen, Bial‐Portela, JABA‐Recordati, Merck Sharp & Dohme, Mylan, Sanofi‐Regeneron e Tecnimede. JSD recebeu honorários por palestras ou ensaios clínicos da Bial, Boehringer Ingelheim, JABA‐Recordati, Merck Sharp & Dohme Portugal, Novo Nordisk, Novartis, Amgen, Sanofi e Tecnimede. PMS recebeu honorários por palestras ou consultoria da Bayer, JABA‐Recordati, Merck Sharp & Dohme Portugal, Kowa Pharmaceuticals, Novartis, Daiichi Sankyo, Amgen, Sanofi‐Regeneron e Tecnimede.
Este estudo teve o apoio da Tecnimede e foi desenvolvido, supervisionado pela Springer Healthcare Communications que colaborou na escrita do artigo e foi responsável pela retribuição pecuniária à comissão científica e ao painel de peritos pelo seu contributo intelectual. A Tecnimede não teve qualquer influência no desenho, elaboração do inquérito, escolha dos membros do painel e interpretação dos resultados. Os autores gostariam de agradecer a Catarina L. Santos, que prestou assistência na redação médica, e a todos os profissionais que constituíram o painel multidisciplinar e que dispensaram algum do seu tempo para responder ao inquérito (Abílio Malheiro, António Ferreira, Carlos Catarino, Davide Carvalho, Diogo Cruz, Elisabete Rodrigues, Elsa Gaspar, Evangelista Rocha, Francisco Araújo, Isabel Nazaré Santos, Isabel Palma, João Porto, João Raposo, Jorge Dores, José Augusto Simões, José Augusto Varandas, José Mendonça, José Pereira de Moura, José Silva Nunes, Luís Andrade, Luísa Maria Sá, Manuela Fiúza, Manuela Silva Melo, Maria Helena Ramos, Mariana Monteiro, Mário Lázaro, Nelson Rodrigues, Paulo Santos, Pedro Monteiro, Pedro Von Hafe, Ricardo Fontes Carvalho, Roberto Palma Reis, Rui Carvalho e Vítor Ramalhinho).




 DCV, doença cardiovascular;
DCV, doença cardiovascular; 
