Estimar os rácios custo‐efetividade e custo‐utilidade da utilização de ticagrelor versus clopidogrel no tratamento de doentes com síndromas coronárias agudas (angina instável, enfarte do miocárdio sem elevação ST [NSTEMI] ou enfarte do miocárdio com elevação ST [STEMI]); incluindo doentes sujeitos a tratamento médico e aqueles geridos com intervenção coronária percutânea (ICP) ou bypass aortocoronário com enxerto (CABG).
MetodologiaFoi utilizada uma árvore de decisão de curto prazo e um modelo de Markov de longo prazo para simular a progressão dos doentes no decurso da sua vida. Os dados de eficácia clínica foram recolhidos a partir do ensaio clínico PLATO e os dados de consumo de recursos foram obtidos na Contabilidade Analítica do Hospital de Santa Marta, legislação dos GDH e consulta de bibliografia disponível.
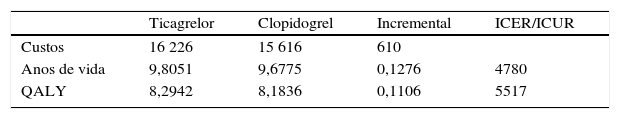
ResultadosTicagrelor proporciona, a cada doente, um incremento de 0,1276 anos de vida e 0,1106QALY. Na perspectiva da sociedade, estes ganhos implicam um aumento da despesa em 610€. Obtêm‐se, assim, um custo incremental por ano de vida salvo de 4780€ e um custo incremental por QALY de 5517€.
ConclusõesOs resultados obtidos mostram que o ticagrelor diminui a quantidade de eventos, quando comparado com clopidogrel. Os custos com ticagrelor são parcialmente compensados por uma diminuição dos custos decorrentes dos eventos evitados. Assim, a utilização de ticagrelor na prática clínica portuguesa é custo‐efetiva quando comparado com a abordagem com clopidogrel.
To estimate the cost‐effectiveness and cost‐utility of ticagrelor in the treatment of patients with acute coronary syndromes (unstable angina or myocardial infarction with or without ST‐segment elevation), including patients treated medically and those undergoing percutaneous coronary intervention or coronary artery bypass grafting.
MethodsA short‐term decision tree and a long‐term Markov model were used to simulate the evolution of patients’ life‐cycles. Clinical effectiveness data were collected from the PLATO trial and resource use data were obtained from the Hospital de Santa Marta database, disease‐related group legislation and the literature.
ResultsTicagrelor provides increases of 0.1276 life years and 0.1106 quality‐adjusted life years (QALYs) per patient. From a societal perspective these clinical gains entail an increase in expenditure of €610. Thus the incremental cost per life year saved is €4780 and the incremental cost per QALY is €5517.
ConclusionsThe simulation results show that ticagrelor reduces events compared to clopidogrel. The costs of ticagrelor are partially offset by lower costs arising from events prevented. The use of ticagrelor in clinical practice is therefore cost‐effective compared to generic clopidogrel.
Ácido acetilsalicílico
Adenosina difosfato
Angina instável
Acidente vascular cerebral
duas vezes por dia
bypass aortocoronário com enxerto
Disease related group
Enfarte agudo do miocárdio
Grupos de diagnóstico homogéneo
Glicoproteína
Rácio custo‐efectividade incremental
Intervenção coronária percutânea
Rácio custo‐utilidade incremental
Instituto Nacional de Estatística
Imposto sobre o valor acrescentado
Enfarte do miocárdio sem elevação ST
Uma vez ao dia
Preço de venda ao público
Ano de vida ajustado pela qualidade
Registo Nacional de Síndromes Coronárias Agudas
Síndromes coronárias agudas
Enfarte do miocárdio com elevação ST
As doenças cardiovasculares constituem a principal causa de morte em Portugal, tendo representado em 2007 32,3% de todos os óbitos (INE, 2008). De entre as mortes de causa cardiovascular, 44,9% são devidas a doença vascular cerebral e 23,1% a doença cardíaca isquémica, com destaque evidente para as síndromas coronárias agudas (SCA) (Alto Comissariado da Saúde, 2007).
A SCA representa uma manifestação potencialmente fatal da aterosclerose normalmente acelerada por trombose aguda, induzida por rutura ou erosão de uma placa aterosclerótica, com ou sem vasoconstrição concomitante, provocando uma redução súbita e crítica do fluxo sanguíneo. Esta rutura desencadeia uma cascata de reações resultando na formação de trombo coronário obstruindo total ou parcialmente o lúmen arterial1,2.
As SCA incluem um grupo de condições clínicas resultantes de doença aterotrombótica coronária em fase instável: enfarte agudo do miocárdio (EAM) com elevação do segmento ST (STEMI), enfarte agudo do miocárdio sem elevação do segmento ST (NSTEMI) e angina instável (AI), cujo principal substrato fisiopatológico comum é a aterosclerose1,2.
Em Portugal, o Registo Nacional de Síndromes Coronárias Agudas (RNSCA) é a principal fonte de informação para a caracterização da patologia. Este registo criado em 2002 visa analisar as características clínicas, o tratamento e o prognóstico dos doentes portugueses com SCA. O RNSCA permite caracterizar a apresentação clínica, a abordagem terapêutica e o prognóstico de todo o espectro de SCA em Portugal e, ainda, avaliar a aplicação das recomendações clínicas para as SCA e monitorizar as variações temporais nas características clínicas, tratamento e prognóstico. Entre 2002‐2009 foram incluídos 22 482 doentes, com idade média de 66±13 anos, 70% do sexo masculino, assim distribuídos: 45,4% com EAM supra‐ST; 41,4% com EAM sem‐ST; 13,1% com angina instável3.
A ativação plaquetária desempenha um importante papel fisiopatológico nas SCA. A ativação plaquetária deve ser considerada não apenas no contexto de uma rutura aguda da placa, mas também como podendo contribuir para eventos aterotrombóticos subsequentes na circulação sistémica em doentes com inflamação da parede arterial. Existem três estratégias relacionadas e complementares que oferecem uma terapêutica antiplaquetária eficaz: inibição da ciclo‐oxigenase (COX)‐1 (ácido acetilsalicílico – AAS), inibição da agregação plaquetária mediada pela adenosina difosfato (ADP) com tienopiridinas (ticlopidina, clopidogrel, prasugrel) e inibição da glicoproteína (GP) IIb/IIIa (tirofiban, eptifibatida, abciximab)4.
O ticagrelor pertence ao grupo farmacoterapêutico dos inibidores da agregação plaquetária excluindo heparina e é o primeiro antagonista do recetor P2Y12 oralmente ativo, reversível, de uma nova classe química, as CPTP5. Como as tienopiridinas, ticagrelor bloqueia o recetor plaquetário ADP P2Y12, de modo a inibir a ativação e agregação plaquetárias mediadas por ADP. Contudo, ao contrário das tienopiridinas, que são antagonistas irreversíveis, o ticagrelor liga‐se direta e reversivelmente ao recetor ADP P2Y12 e, de modo não competitivo, inibe a transdução do sinal.
MétodosO presente estudo avalia as relações de custo‐efetividade e custo‐utilidade de ticagrelor (dose de carga +90mg bid) face ao clopidogrel (dose de carga +75mg od), no tratamento de doentes com SCA.
As consequências foram medidas em anos de vida salvos e anos de vida ajustados pela qualidade (QALY). Os dados de eficácia foram retirados do ensaio clínico PLATO. Os eventos principais do modelo são as mortes por qualquer causa, enfarte do miocárdio e AVC não fatais.
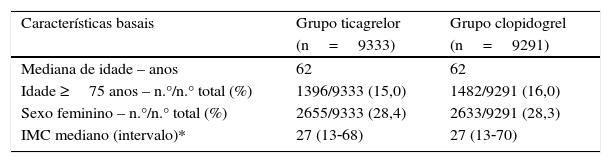
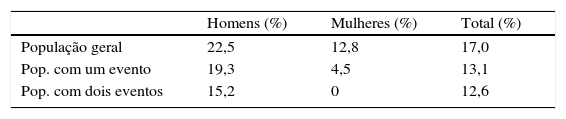
As características mais importantes da população de base considerada no modelo, baseada nos doentes do ensaio PLATO, constam da Tabela 1.
Características da população no cenário base
| Características basais | Grupo ticagrelor | Grupo clopidogrel |
| (n=9333) | (n=9291) | |
| Mediana de idade – anos | 62 | 62 |
| Idade ≥75 anos – n.°/n.° total (%) | 1396/9333 (15,0) | 1482/9291 (16,0) |
| Sexo feminino – n.°/n.° total (%) | 2655/9333 (28,4) | 2633/9291 (28,3) |
| IMC mediano (intervalo)* | 27 (13‐68) | 27 (13‐70) |
* O índice de massa corporal (IMC) é o peso em quilogramas dividido pelo quadrado da altura em metros.
Foi considerado um horizonte temporal coincidente com o tempo de vida dos doentes para permitir a avaliação a longo prazo do impacto da terapêutica nos resultados de saúde e nos custos associados.
A avaliação é realizada na perspetiva da sociedade, de acordo com as recomendações constantes das «orientações metodológicas para estudos de avaliação económica»6, onde custos e consequências para todas as partes envolvidas são tomados em conta, incluindo os custos indiretos.
Eficácia clínicaO ensaio PLATO7 consistiu num ensaio aleatorizado, multicêntrico, com dupla‐ocultação, que avaliou a administração de ticagrelor (180mg dose de carga, seguido de 90mg duas vezes ao dia) e clopidogrel (300‐600mg dose de carga, seguido de 75mg/dia) na prevenção de eventos cardiovasculares em 18 624 doentes admitidos no hospital com SCA, com ou sem elevação do segmento ST.
A variável primária de eficácia foi um endpoint composto (morte por causa vascular, EAM ou AVC) medido em número de eventos ocorridos. Aos 12 meses, ticagrelor reduziu a ocorrência da variável primária de eficácia comparativamente ao clopidogrel: 9,8 versus 11,7% (HR=0,84; IC 95% 0,77‐0,92, p<0,001).
Modelo adotadoO modelo do Brilique® utilizado na análise consistiu numa adaptação ao caso português de um modelo desenvolvido internacionalmente e que foi originalmente publicado no EHJ por Nikolic et al.8 Este modelo foi já objeto de várias publicações internacionais. É um modelo em duas partes: uma árvore de decisão cobrindo o período inicial de um ano, baseada nos dados do estudo PLATO e um modelo de Markov para a extrapolação dos resultados a longo‐prazo. A duração de cada ciclo no modelo de Markov é de um ano. Esta construção é semelhante aos modelos analíticos de decisão recentes na área das SCA9–11.
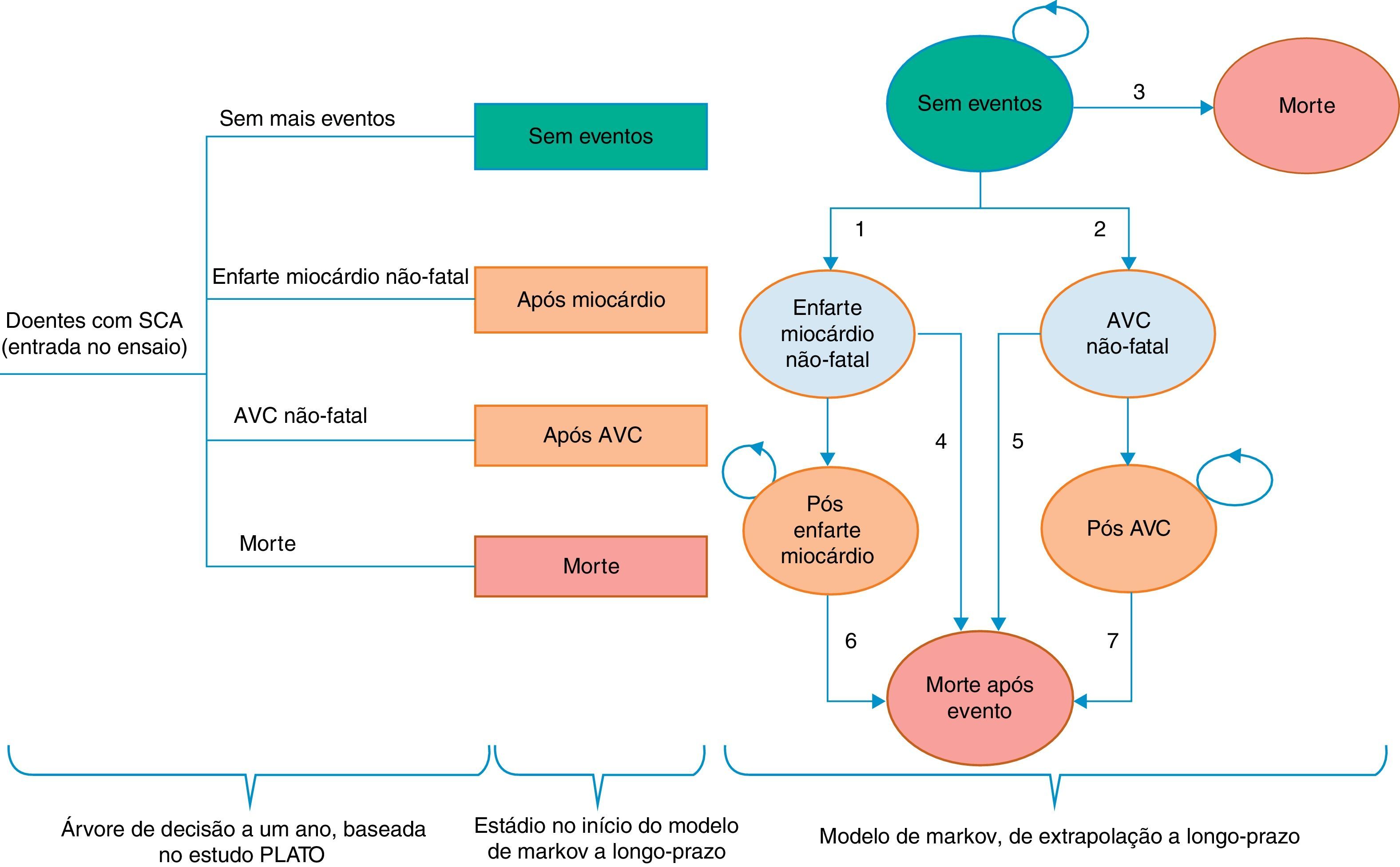
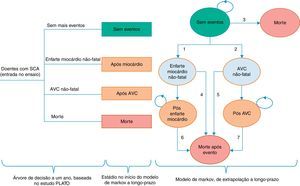
A Figura 1 mostra a estrutura do modelo: árvore de decisão e modelo de Markov.
Estrutura do modelo. Adaptado de Nikolic et al.8
No primeiro ano os doentes são alocados aos diferentes nódulos da árvore de decisão, de acordo com as probabilidades estimadas de sofrerem cada evento. Estas vão diferir entre as duas estratégias de tratamento, de acordo com o efeito do tratamento observado no ensaio PLATO. Cada nódulo da árvore de decisão está associado a uma estimativa de consumo de cuidados de saúde e QALY.
Após o primeiro ano (árvore de decisão), assume‐se que o tratamento com ticagrelor ou clopidogrel terminou em ambos os ramos, sem repercussões diretas (efeitos de tratamento ou efeitos de recaída) para os tratamentos nos restantes ciclos de Markov.
Os ciclos de Markov têm uma duração anual. A cada estado de saúde está associada uma estimativa de qualidade de vida relacionada com a saúde na forma de QALY e outra de consumos de cuidados de saúde. A coorte de doentes progride através do modelo de Markov de acordo com as probabilidades de transição estimadas, a partir dos dados do ensaio clínico PLATO.
Em cada ano os doentes «Sem eventos» têm um risco de sofrer um enfarte do miocárdio não fatal ou um AVC não fatal (transições 1 e 2). Se ocorrer um evento não fatal, os doentes transitam para o nódulo «Enfarte do miocárdio não fatal» ou «AVC não fatal». Doentes no nódulo «Sem eventos» estão também sujeitos a um risco de morte todos os anos (transição 3). Se ocorrer um evento fatal, os doentes fazem a transição para o nódulo «Morte». Este é um nódulo de saúde «absorvente», no sentido em que transições posteriores não são permitidas após entrada neste estado.
Os nódulos «Enfarte do miocárdio não fatal» e «AVC não fatal» representam o prognóstico do primeiro ano em termos de sobrevivência, custos e qualidade de vida de doentes que sofram um evento não fatal. Nos nódulos de «Enfarte do miocárdio não fatal» e «AVC não fatal» os doentes enfrentam um risco de morte e de transitarem para o nódulo «Morte após evento» (transições 4 e 5). Os nódulos de «Enfarte do miocárdio não fatal» e «AVC não fatal» são nódulos «túnel», dado que os doentes só podem permanecer nestes nódulos por um ciclo. Doentes que ainda estejam vivos decorrido um ano fazem a transição para os nódulos «Pós‐enfarte do miocárdio» e «Pós‐AVC». Estes dois nódulos são semelhantes aos nódulos «Enfarte do miocárdio não fatal» e «AVC não fatal» e representam o prognóstico em termos de sobrevivência, custos e qualidade de vida dos doentes no segundo ano, e subsequentes, após um evento não fatal posterior à entrada no estudo PLATO.
Os nódulos «Pós‐enfarte do miocárdio» e «Pós‐AVC», além de estarem associados a custos e a QALY, estão associados a um risco de morte (transições 6 e 7).
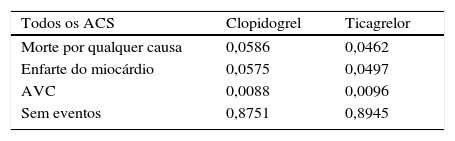
Calibração do modelo a curto prazoNa calibração do modelo a curto prazo, as probabilidades baseiam‐se nos dados do estudo PLATO (Tabela 2). Foram obtidos quatro parâmetros de transição para calibrar os nódulos da árvore de decisão:
- 1.
A probabilidade de um enfarte do miocárdio não fatal.
- 2.
A probabilidade de um AVC não fatal.
- 3.
A probabilidade de morte, por qualquer causa.
- 4.
A probabilidade de não ter mais nenhum evento, definida como a diferença entre um e a soma das probabilidades de ocorrência dos outros três eventos.
No final do primeiro ano há diferenças na distribuição da população pelos diversos nódulos entre os doentes tratados com ticagrelor e os tratados com clopidogrel. Na modelização a longo prazo já não há doentes a serem tratados com ticagrelor, pelo que as probabilidades de transição são idênticas para os dois braços de tratamento. Assim, mesmo com probabilidades de transição idênticas, os efeitos a longo prazo diferem entre os braços de tratamento porque as transições se fazem a partir de diferentes pontos iniciais.
Os riscos de morte anuais no nódulo «Sem eventos» (transição 3) são estimados usando taxas de mortalidades padronizadas por idade, provenientes das tábuas de mortalidade portuguesas12. Deve ser tido em conta que doentes no nódulo «Sem eventos» têm estado livres de eventos durante pelo menos um ano desde o evento SCA inicial. A evidência sugere que doentes que sofreram um evento SCA têm um risco relativo superior de sofrerem um evento fatal no ano seguinte e que este decresce quanto mais tempo passa desde o evento SCA inicial13,14. Aplicou‐se um hazard ratio de 2 às taxas de mortalidade, por idade e género, para incorporar o risco de mortalidade acrescido associado às SCA. Assumiu‐se um desvio padrão de 0,10 para o logaritmo do hazard ratio para a análise probabilística de sensibilidade e que este ratio segue uma distribuição normal na escala logarítmica.
Para o nódulo «Enfarte do miocárdio não fatal» (transição 4), comparou‐se o risco de mortalidade observado no estudo PLATO ao risco nas tábuas de mortalidade, tendo‐se aplicado um risco acrescido de morte com um hazard ratio de 6. Assumiu‐se um desvio padrão do logaritmo do hazard ratio de 0,3 para a análise probabilística e uma distribuição normal na escala logarítmica.
Para o nódulo de «AVC não‐fatal» (transição 5) foram usados dois estudos internacionais que forneceram o risco relativo de morte para o primeiro ano após o AVC comparado com pessoas de idade e sexo similar na população geral15–17. O estudo de Dennis et al.16, com um risco de 7,43, foi considerado o mais robusto já que tinha o período de follow‐up mais longo e o maior número de doentes. Dado existirem numericamente mais ACS na população tratada com Brilique®, decidiu‐se usar o valor de 7,43 para manter a análise conservadora no que diz respeito à estratégia Brilique®. Foi assumido na escala logarítmica um desvio padrão de 0,35.
No que concerne à transição de «pós‐enfarte do miocárdio» para «Morte» (transição 6), assume‐se que, já que um doente no nódulo de saúde «Pós‐enfarte do miocárdio» tem já um enfarte recorrente, este doente tem um risco de mortalidade superior a um doente no nódulo «Sem eventos». Um doente no nódulo «Pós‐enfarte do miocárdio» já sobreviveu um ano após o seu evento recorrente e apresenta um risco de mortalidade inferior ao dos doentes no nódulo «Enfarte do miocárdio não fatal». Parece provável então que o risco de mortalidade para doentes no nódulo «Pós‐enfarte do miocárdio» esteja entre o de mortalidade no nódulo «Sem eventos» e no nódulo «Enfarte do miocárdio não fatal». Assim, foi aplicada na análise um hazard ratio de 3, para garantir consistência lógica dos valores dos parâmetros do modelo. Assumiu‐se um desvio padrão de 0,15 na escala logarítmica para uso na análise de sensibilidade probabilística.
Para o nódulo «Pós‐AVC» (transição 7), os estudos identificados mostram um elevado nível de consistência quanto ao risco relativo de morte no segundo, e anos subsequentes, após o primeiro AVC18. Selecionou‐se o valor de 2,07 de Dennis et al.16 (1993) como o risco relativo de morte no primeiro ano, para o segundo ano e anos subsequentes o risco relativo é a média dos restantes anos de seguimento o que foi consistente do 2.° ano em diante. Assumiu‐se na análise probabilística uma distribuição normal com desvio padrão de 0,10 na escala logarítmica.
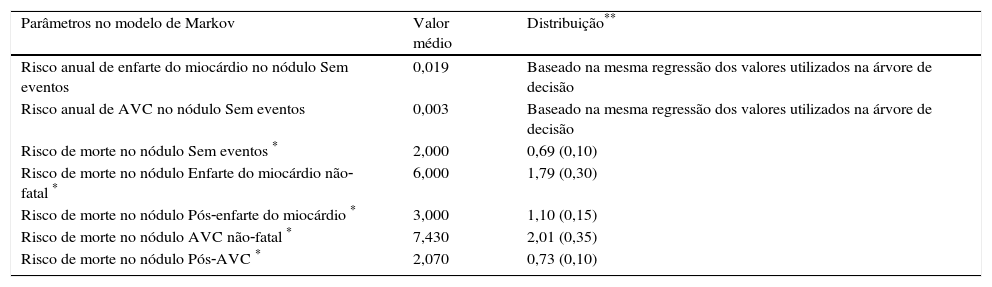
Os parâmetros de transição do modelo de Markov, no cenário base, estão sumariados na Tabela 3.
Parâmetros de transição para o modelo de Markov
| Parâmetros no modelo de Markov | Valor médio | Distribuição** |
| Risco anual de enfarte do miocárdio no nódulo Sem eventos | 0,019 | Baseado na mesma regressão dos valores utilizados na árvore de decisão |
| Risco anual de AVC no nódulo Sem eventos | 0,003 | Baseado na mesma regressão dos valores utilizados na árvore de decisão |
| Risco de morte no nódulo Sem eventos * | 2,000 | 0,69 (0,10) |
| Risco de morte no nódulo Enfarte do miocárdio não‐fatal * | 6,000 | 1,79 (0,30) |
| Risco de morte no nódulo Pós‐enfarte do miocárdio * | 3,000 | 1,10 (0,15) |
| Risco de morte no nódulo AVC não‐fatal * | 7,430 | 2,01 (0,35) |
| Risco de morte no nódulo Pós‐AVC * | 2,070 | 0,73 (0,10) |
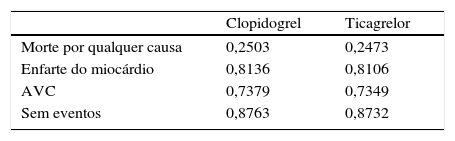
As estimativas de utilidade usadas em cada nódulo da árvore de decisão baseiam‐se nos resultados da aplicação do EQ‐5D12, no estudo PLATO.
Os QALY médios para cada nódulo na árvore de decisão foram estimados usando regressões OLS, com os nódulos e grupos de tratamento introduzidos como variáveis dummy. As equações incluem nas variáveis explicativas a idade e o género, de forma a possibilitar a estimativa de QALY para diferentes idades e para homens e mulheres separadamente.
Os QALY médios estimados, por nódulo na árvore de decisão e por grupo de tratamento, são apresentados na Tabela 4.
Utilidades no modelo a longo prazoPara o nódulo «Sem eventos», foi usada a estimativa de QALY para doentes sem eventos do ensaio clínico PLATO. Foi utilizada para este parâmetro a estimativa média para o ticagrelor e para o clopidogrel (0,875) para doentes com menos de 70 anos. Quando o modelo é analisado para homens e mulheres separadamente a estimativa dos QALY utilizada para os homens é cerca de 0,05 superior à das mulheres e varia com a idade de início da coorte. À medida que os doentes envelhecem no modelo é aplicado um decremento devido à idade.
As estimativas de QALY para o modelo de Markov estão sumarizadas na Tabela 5.
Estimativas de QALY para o modelo de Markov
| Parâmetros no Modelo de Markov | Valor médio |
| Score de QALY no nódulo Sem evento, idade<70 | 0,8748 |
| Score de QALY no nódulo Sem evento, idade 70‐79 | 0,8400 |
| Score de QALY no nódulo Sem evento, idade>79 | 0,7814 |
| Decremento do score de QALY no nódulo Enfarte miocárdio não‐fatal | 0,0627 |
| Decremento do score de QALY no nódulo Pós‐enfarte miocárdio | 0,0627 |
| Decremento do score de QALY no nódulo AVC não‐fatal | 0,1384 |
| Decremento do score de QALY no nódulo Pós‐AVC | 0,1384 |
O desenho do modelo apenas permitiu que os custos indiretos fossem adicionados aos eventos no primeiro ano, o que constituiu uma subestimativa dos efeitos da morbilidade na produtividade da população, já que alguns eventos relevantes só ocorrerão após o primeiro ano.
As produtividades médias anuais em 2010 estimadas para o grupo etário acima de 60 anos foram 15 743€ para os homens e 10 839€ para mulheres sendo as produtividades médias diárias de 68,50€ e 47,12€, respetivamente. Não se atualizaram estes valores para 2012, o que parece razoável tendo em conta a evolução do mercado de trabalho e das remunerações em Portugal nos últimos anos.
Assumiu‐se que o absentismo associado a um evento corresponde a um número de dias úteis igual à demora média hospitalar e a mais duas vezes essa duração para a convalescença. Usando os GDH de 2009 obtém‐se uma demora média para os sobreviventes do AVC de 10,3 dias e a do EAM de 7,9 dias. O absentismo é então de 30,9 dias para o AVC e de 23,7 dias para o EAM, sendo os custos respetivos dados pelo produto dos dias, do custo diário e da taxa de emprego após evento.
As taxas de emprego consideradas no cálculo são constantes da Tabela 6.
Para o custo da redução do emprego devido à reforma antecipada fez‐se o pressuposto de uma saída do mercado de trabalho levar, em média, a menos 2,5 anos de emprego, o que corresponde a um exemplo em que a idade média considerada na análise é 62,5 anos e a reforma normal aos 65.
Custos de ticagrelor e do comparador clopidogrelO tratamento com ticagrelor deve ser iniciado com uma dose de carga única de 180mg (dois comprimidos de 90mg) e depois continuada com 90mg duas vezes ao dia. Desta forma, o custo diário do ticagrelor é de 2,67€ (PVP sem IVA).
O custo diário do clopidogrel, o qual no momento da análise era 0,32€, foi estimado assumindo uma dose diária de 75mg custeada ao preço de referência do grupo homogéneo correspondente (GH0736), sem IVA.
Outros custos diretosOs restantes custos diretos, incluem os custos relacionados com a utilização dos serviços de saúde, ou seja, internamentos, consultas, outros medicamentos, exames de diagnóstico, terapêuticas várias, etc. Os custos do modelo, por nódulo, foram estimados separadamente para o ciclo inicial (1.° ano) e para os ciclos subsequentes.
Para o primeiro ano foram utilizados os custos unitários portugueses e o consumo de recursos registrados no ensaio clínico PLATO. Para os ciclos seguintes foi utilizada uma atualização das estimativas de custos diretos gerados no primeiro ano.
Na medida em que existem diferenças entre as estimativas baseadas no PLATO e as estimativas precisas para padrões típicos de consumo no contexto do sistema de saúde português, foi realizada análise de sensibilidade a estes parâmetros.
As estimativas dos custos unitários são genericamente baseadas na legislação dos GDH.
Foi também utilizada informação da Contabilidade Analítica do Hospital de Santa Marta, Serviços de Cardiologia e Cirurgia Cardio‐Torácica.
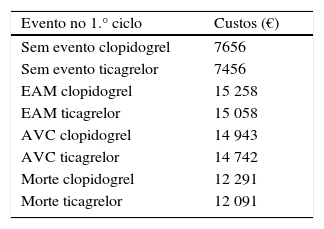
Os resultados, com base em dados portugueses de custos unitários e padrões de consumo do ensaio clínico PLATO constam da Tabela 7.
Para os ciclos seguintes, foi utilizada uma atualização de estimativas dos custos diretos gerados no primeiro ano e para os anos seguintes para os casos do EAM e para o AVC (Tabela 8).
Custos diretos após primeiro ano no cenário base
| Custos diretos dos nódulos do modelo e medicamentos | Custos (€) |
| Custo «Enfarte miocárdio» no 1.° ano modelo de Markov | 7834,74 |
| Custo «Enfarte miocárdio» no 2.° e anos subsequentes modelo de Markov | 772,36 |
| Custo «AVC» no 1.° ano modelo de Markov | 7220,99 |
| Custo «AVC» no 2.° e anos subsequentes modelo de Markov | 531,37 |
| Custo do nódulo «Sem eventos» no modelo de Markov | 651,87 |
O cenário de base tem um horizonte temporal de análise coincidente com a esperança de vida e uma taxa de atualização de 5%, de acordo com as orientações metodológicas para estudos de avaliação económica.
Análise de sensibilidade univariadaA análise de sensibilidade destina‐se a verificar a robustez dos resultados em relação aos pressupostos da análise, em particular relativamente àqueles para os quais a informação disponível é mais incerta. Foi realizada análise de sensibilidade univariada, ao horizonte temporal, à não inclusão dos custos indiretos, a valores alternativos para a taxa de atualização e, por fim, a custeios alternativos dos eventos vasculares. Os resultados de custo‐efetividade e de custo‐utilidade mostraram ser robustos na medida em que em todos os cenários indicados os valores dos rácios incrementais (ICER e rácio custo‐utilidade incremental [ICUR]) permaneceram a níveis aceitáveis (abaixo dos 20 000€/QALY).
Análise de sensibilidade probabilísticaNa análise probabilística foi utilizada uma simulação de Monte‐Carlo de segunda ordem para propagar a incerteza a partir dos inputs individuais do modelo (single model inputs) ao longo deste, de forma a que a incerteza nos resultados de custo‐efetividade reflita a incerteza na decisão de implementar uma estratégia de tratamento e não a incerteza em torno dos inputs individuais do modelo19,20. A distribuição combinada dos custos e QALY incrementais é representada graficamente no plano de custo‐utilidade. Os resultados apresentados na Figura 2 basearam‐se em 10 000 simulações do modelo.
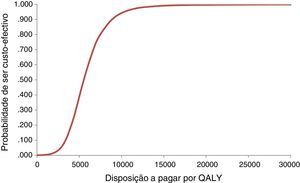
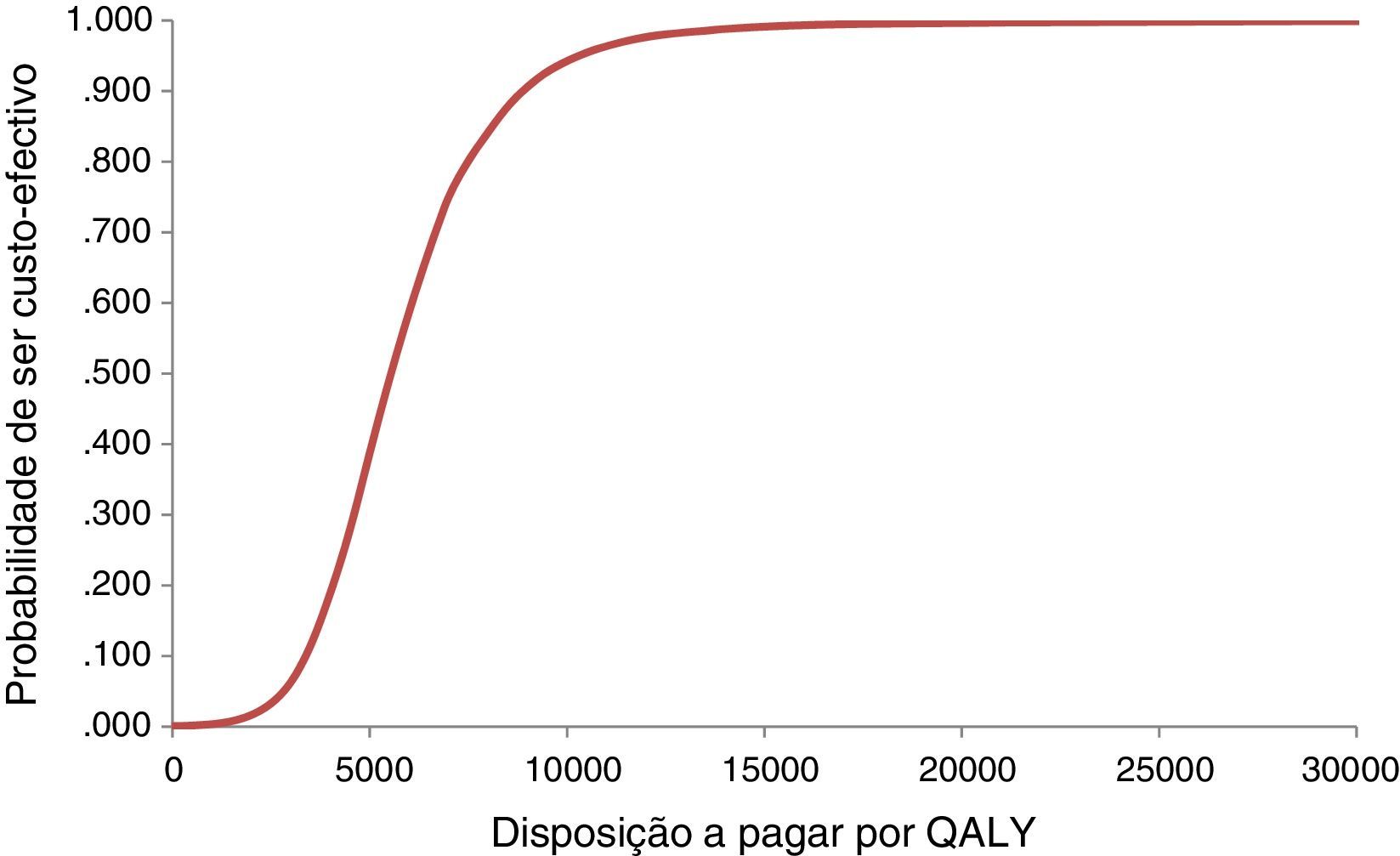
Foram igualmente estimadas as probabilidades de ticagrelor® ser custo‐efetivo a diferentes níveis da disposição a pagar por um QALY, ou seja, os valores da curva de aceitabilidade20 (Figura 3).
O ICUR médio simulado foi 5517€. Para uma disposição a pagar de 5541€ há uma probabilidade de aceitação de 50%. Os limites de um intervalo de 95% são 2314€ para percentil 2,5% e 11 790€ para o percentil 97,5%, muito abaixo do limiar de aceitabilidade usual, de 20 000€.
DiscussãoOs resultados mostraram ser robustos numa variedade de análises unidimensionais e num conjunto de cenários alternativos. Nalguns casos, quando se alteram as fontes das estimativas de custos dos eventos (p. ex.: considerando nulos os custos indiretos), os valores dos rácios incrementais são mais altos, mas apenas ligeiramente, já que os rácios aumentam apenas 2,4%. Quando se reduz o horizonte de análise os resultados mostram rácios incrementais superiores com uma duplicação do valor do cenário base. Nestes casos ocorre uma modificação percentualmente significativa dos ICER/ICUR, mas mesmo nos piores cenários continuamos a ter indicadores de custo‐efetividade/custo‐utilidade abaixo dos 20 000€ por QALY (Tabela 9).
ConclusõesTodos os resultados apurados para a avaliação económica resultante da comparação entre o ticagrelor e o clopidogrel na prevenção secundária após eventos vasculares mostram que o ticagrelor tem excelentes níveis de custo efetividade, gerando ganhos de saúde a custos muito abaixo dos limiares aceitáveis para a disposição a pagar do SNS.
Os resultados mostraram ser robustos numa variedade de análises unidimensionais e num conjunto de cenários alternativos.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram que não aparecem dados de pacientes neste artigo.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
FinanciamentoA Astrazeneca financiou a adaptação deste estudo para Portugal. Não existiu por parte da entidade financiadora qualquer influência sobre os autores do estudo que condicionasse a obtenção de resultados.
Conflito de interessesOs autores declaram não haver conflito de interesses.


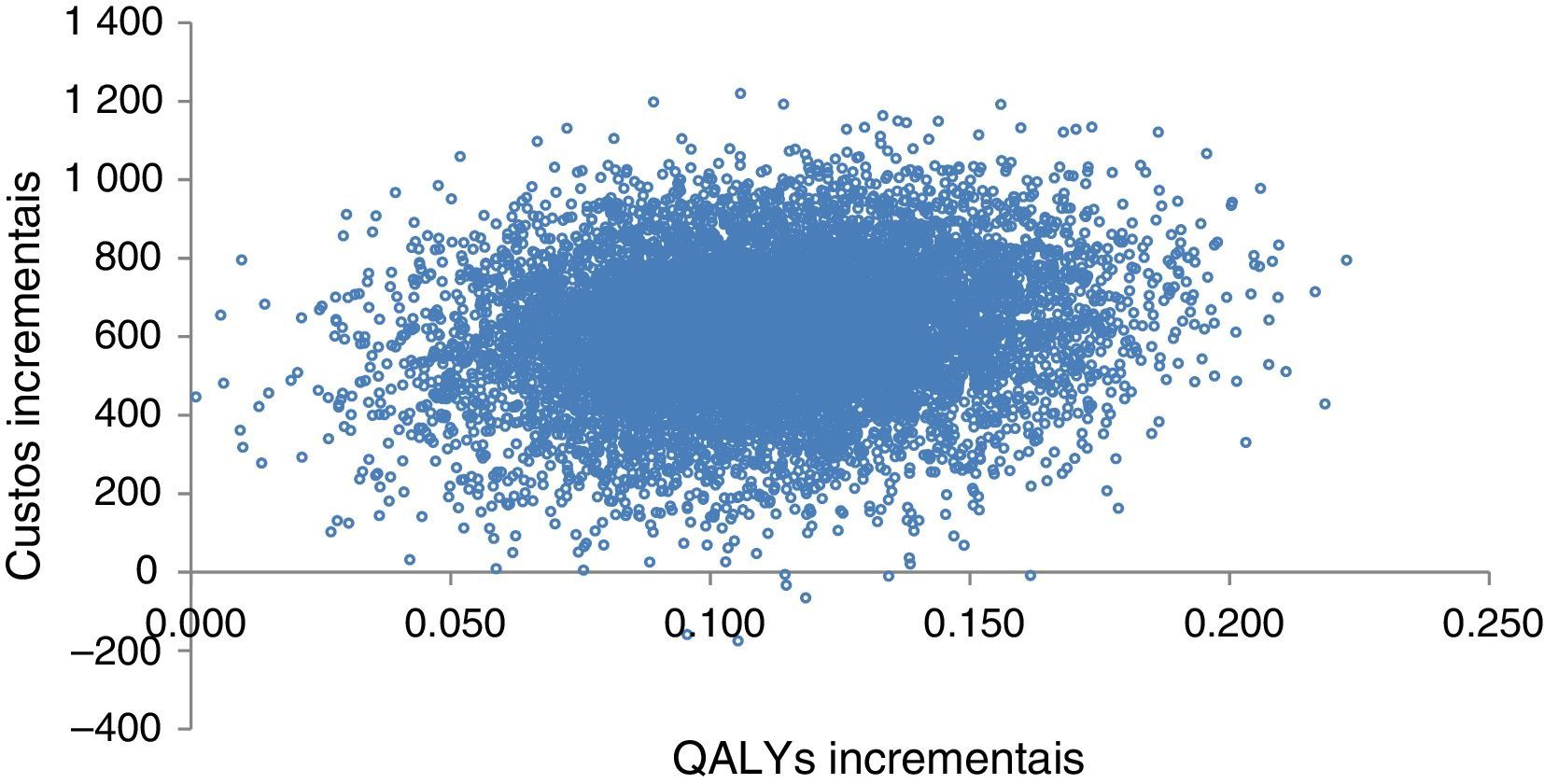


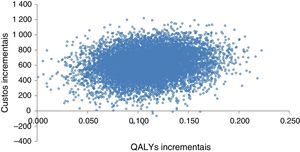 QALY incrementais.' title='Dispersão dos custos e
QALY incrementais.' title='Dispersão dos custos e